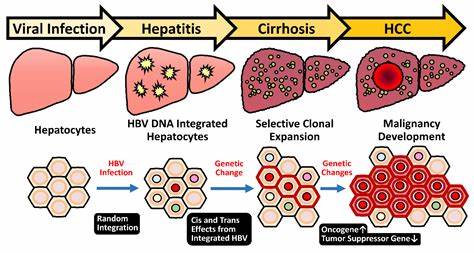
Die Rolle des Hepatitis-B-Virus-Genoms und seiner Integration in das hepatozelluläre Karzinom Hepatozelluläres Karzinom (HCC) ist eine der häufigsten und tödlichsten Krebsarten weltweit. Es entwickelt sich in der Leber und ist oft mit chronischen Erkrankungen, insbesondere mit einer Infektion durch das Hepatitis-B-Virus (HBV), verbunden. Ein faszinierender Aspekt der HBV-Infektion ist die Fähigkeit des Virus, sich in das Genom der Leberzellen zu integrieren, was erhebliche Auswirkungen auf die Entstehung von Krebs hat. HBV gehört zur Familie der Hepadnaviren und infiziert hauptsächlich Leberzellen. Mit einem kleinen, zirkulären, doppelsträngigen DNA-Genom ist HBV besonders dafür bekannt, dass es sich in das Genom der Wirtszellen integriert.
Diese Integration kann bereits in frühen Phasen der Infektion auftreten und ist ein entscheidender Faktor bei der Entwicklung von HCC. Epidemiologische Studien zeigen, dass Menschen mit HBV-Infektion ein bis zu 15-fach höheres Risiko haben, an Leberkrebs zu erkranken. Dies liegt nicht nur an den bestehenden Leberschäden, sondern auch an den genetischen Veränderungen, die durch die Virusintegration hervorgerufen werden. Ein zentraler Mechanismus, durch den HBV zur Krebsentstehung beiträgt, ist die Induktion von Genominstabilität. Wenn HBV-DNA in das Genom einer Leberzelle integriert wird, kann dies zu strukturellen Variationen in den Chromosomen führen.
Diese Variationen umfassen Translokationen und Deletionen, die die normale Genexpression stören können. Besonders das HBx-Protein, ein wichtiges Produkt des HBV, hat sich als krebserregend erwiesen. Es aktiviert signaltransduzierende Pfade, die zu einer übermäßigen Zellproliferation führen können, und beeinflusst auch die Tumorsuppressorgene, die normalerweise das Wachstum von Tumoren verhindern. Die Integration von HBV findet oft an sogenannten „Hotspots“ im menschlichen Genom statt, insbesondere in Regionen, die als fragile Stellen bekannt sind. Diese Hotspots sind besonders anfällig für genetische Veränderungen und werden häufig mit der Entstehung von Tumoren in Verbindung gebracht.
Dazu gehört unter anderem die Aktivierung von Onkogenen wie TERT und CCNE1, die das Wachstum und die Überlebensfähigkeit von Krebszellen fördern. Die Bedeutung dieser Hotspots ist ein aktives Forschungsfeld, da das Verständnis der genauen Integrationsmechanismen zu neuen Ansätzen in der Krebsbehandlung und -diagnose führen könnte. Die Behandlung von HBV-Infektionen und die Prävention von HCC hat in den letzten Jahren Fortschritte gemacht. Aufgrund der Natur des Virus und seines Verhaltens im Wirtsorganismus ist die Herausforderung jedoch, die virale Integration und die daraus resultierenden genetischen Änderungen vollständig zu verstehen und zu beseitigen. Aktuelle Therapien konzentrieren sich auf die Suppression der Virusvermehrung, ohne jedoch das Problem der bereits integrierten HBV-DNA zu lösen.
Dies lässt die Möglichkeit offen, dass trotz erfolgreicher Virusbekämpfung ein Risiko für die Entstehung von HCC bestehen bleibt. Ein vielversprechender Ansatz zur Erforschung der Virusintegration ist die Anwendung fortschrittlicher Sequenzierungstechnologien. Diese Methoden ermöglichen es, die genaue Sequenz und die Folgen der Integration von HBV-DNA in das menschliche Genom zu analysieren. Dank dieser Technologien können Forscher nicht nur die heterogenen Integrationsmuster besser verstehen, sondern auch deren Auswirkungen auf die Genexpression in betroffenen Leberzellen. Zudem bietet die CRISPR/Cas9-Technologie neue Perspektiven für die gezielte Bearbeitung von Genen, um integrierte Virussequenzen zu eliminieren.
Der Einsatz dieser Technologie könnte einen paradigmatischen Wandel in der Behandlung von HBV-Infektionen darstellen, indem man nicht nur die Viruslast reduziert, sondern auch die Ursachen für die Genominstabilität angeht, die zur Entwicklung von HCC führt. Solche therapeutischen Innovationen sind entscheidend, um die Mortalität durch Leberkrebs zu reduzieren und langfristige Lösungen zu finden. Trotz der Fortschritte in der Forschung bleibt die Untersuchung der genauen Mechanismen, durch die HBV zur Krebsentstehung beiträgt, von größter Bedeutung. Jüngste Studien haben gezeigt, dass die genetische Variabilität von HBV-Genomen und deren Interaktionen mit menschlichen Genen komplex sind. Diese Komplexität erklärt, warum einige HBV-Infizierte kein HCC entwickeln, während andere dies trotz ähnlicher Viruslast tun.
Ein besseres Verständnis dieser Beziehungen könnte zur Identifizierung von Biomarkern führen, die es ermöglichen, Personen mit einem höheren Risiko für die Entstehung von HCC frühzeitig zu identifizieren. Die Rolle des HBV-Genoms in der Krebsentstehung ist ein Beispiel für die Wechselwirkungen zwischen Virus und Wirtsgenom, die in der modernen Medizin zunehmend an Bedeutung gewinnen. Mit der Entwicklung vielfältiger Forschungsansätze und Technologien, die das Virusthema und die Krebsforschung verbinden, eröffnen sich neue Horizonte. Das Ziel ist es, nicht nur diagnostische Werkzeuge zu entwickeln, sondern auch innovative Therapieansätze zur Bekämpfung von HBV-bedingtem Leberkrebs zu fördern. Zusammenfassend lässt sich sagen, dass die Integration des Hepatitis-B-Virus-Genoms in Leberzellen eine Schlüsselrolle bei der Entstehung von Leberkrebs spielt.
Die Aufklärung der Mechanismen und die Entwicklung effektiver Therapieansätze sind dringend erforderlich, um die Gesundheitskrise, die durch HBV-Infektionen verursacht wird, zu bewältigen. In den kommenden Jahren könnte die Forschung auf diesem Gebiet nicht nur zu Leben rettenden Therapien führen, sondern auch wertvolle Einblicke in die Grundlagen der Onkologie im Allgemeinen bieten.