Die weltweite Zunahme von Übergewicht und Adipositas stellt eine erhebliche gesundheitliche Herausforderung dar. Zahlreiche Studien haben sich damit beschäftigt, wie Ernährungsinterventionen den Stoffwechsel verbessern und Gewichtsverlust fördern können. Neben bekannten Ansätzen wie der Reduzierung von Kohlenhydraten und Fetten richtet sich der Fokus immer stärker auf die Rolle einzelner Aminosäuren, insbesondere Cystein, einem schwefelhaltigen Nicht-Essentiellen Aminosäure, die essenzielle Funktionen im Körper erfüllt. Neueste Forschungen zeigen, dass der gezielte Entzug von Cystein im Experiment mit Mäusen zu einem dramatischen und raschen Gewichtsverlust führt – was neue Perspektiven für die Behandlung von Stoffwechselerkrankungen und Fettleibigkeit eröffnet. Cystein ist für den Körper nicht nur eine Baustein für Proteine, sondern auch kritisch für die Synthese von Glutathion (GSH), eines der wichtigsten Antioxidantien, die Zellen vor oxidativem Stress schützen.
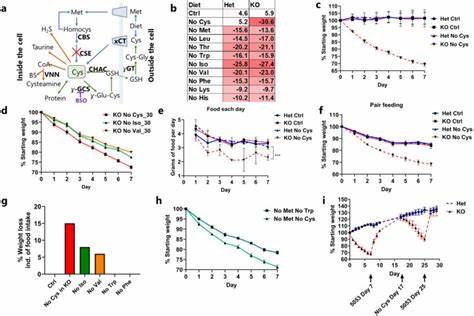
Darüber hinaus spielt Cystein eine entscheidende Rolle in der Produktion von Coenzym A (CoA), einem Kofaktor, der zentral für zahlreiche Stoffwechselwege, insbesondere für die Energiegewinnung in den Mitochondrien, ist. Trotz seiner bedeutenden Funktionen wird Cystein üblicherweise nicht zu den essenziellen Aminosäuren gezählt, da der Körper es normalerweise selbst synthetisieren kann. Allerdings können genetische Störungen in den Enzymen der Transsulfurierungs-Route diese Eigenproduktion behindern, wodurch Cystein zu einer essentiellen Nährstoffquelle wird. In Untersuchungen mit genetisch veränderten Mäusen, denen die Fähigkeit zur Endogenproduktion von Cystein fehlt (Cse-Knockout-Mäuse), hat die Ernährung mit cysteinfreier Nahrung innerhalb von nur sieben Tagen zu einem Gewichtsverlust von bis zu 30 Prozent geführt. Im Gegensatz zu anderen essentiellen Aminosäuren zeigt die Cysteinrestriktion die stärksten Effekte auf das Körpergewicht.
Interessanterweise ist dieser Gewichtsverlust reversibel, was bedeutet, dass die Tiere nach Wiedereinführung von Cystein ihre ursprüngliche Körpermasse schnell wiedererlangen. Die zugrunde liegenden Mechanismen dieses Phänomens sind vielschichtig. Der Mangel an Cystein führt zu einer Aktivierung der sogenannten integrierten Stressantwort (ISR) und der oxidativen Stressantwort (OSR). Beide Mechanismen wirken synergistisch und erhöhen die Produktion von Stresshormonen wie GDF15 und FGF21, die den Energiehaushalt und Appetit regulieren und so zur Gewichtsreduktion beitragen. Diese Stressantworten hemmen gleichzeitig die Proteinsynthese und verschieben den Fokus des Stoffwechsels hin zu energieineffizientem anaerobem Glykolyse-Stoffwechsel.
Dabei wird weniger Energie aus der Nahrung effizient genutzt, was den Energieverbrauch erhöht und den Gewichtsverlust beschleunigt. Neben der Abnahme des Glutathion-Spiegels konnte auch ein signifikanter Rückgang der Coenzym A-Level in verschiedenen Geweben beobachtet werden. CoA, das bei der Umsetzung von Fettsäuren und Kohlenhydraten zu Energie eine zentrale Rolle spielt, wird durch den Mangel an Cystein in seiner Biosynthese beeinträchtigt. Dies resultiert in einer verminderten mitochondrialen Funktionalität und einem gestörten Tricarbonsäurezyklus (TCA-Zyklus), was die metabolische Effizienz weiter senkt. Gleichzeitig werden Stoffwechselzwischenprodukte wie Pyruvat, Orotate und verschiedene Aminosäuren vermehrt mit dem Urin ausgeschieden, was auf eine ineffiziente Nutzung der Nährstoffe hinweist.
Die metabolische Anpassung an Cysteinmangel beinhaltet auch eine selektive Verbrennung von Fettdepots. Studien dokumentieren eine deutliche Reduktion des Fettgewebes in unter Cysteinmangel stehenden Tieren, begleitet von einer sogenannten „Browning“ des weißen Fettgewebes. Dieser Prozess verwandelt energiespeicherndes weißes Fett in thermogenes braunes oder beiges Fettgewebe, das durch vermehrte Aktivität von Proteinen wie Uncoupling Protein 1 (UCP1) die Wärmeproduktion steigert. Da keine erhöhte körperliche Aktivität der Mäuse festgestellt wurde, ist die thermogene Komponente eine Schlüssellinie für die gesteigerte Energieverbrennung und den schnellen Fettabbau. Wichtig ist dabei, dass die beobachteten Gewichtsveränderungen nicht ausschließlich durch reduzierte Nahrungsaufnahme erklärt werden können.
Obwohl die Mäuse auf cysteinfreien Diäten weniger Nahrung zu sich nahmen, zeigte die Restriktion von Cystein im Gegensatz zu anderen Aminosäuredefiziten einen überproportionalen Gewichtsverlust, der die alleinige Wirkung eines Kaloriendefizits ausschließt. Dies unterstreicht die einzigartige Rolle von Cystein in der Regulation des Energiehaushalts. Genetische Studien, bei denen die entsprechenden Gene für die Stresshormone GDF15 und FGF21 ausgeschaltet wurden, zeigen eine abgeschwächte Gewichtverlustreaktion auf den Cysteinmangel. Dies bestätigt, dass diese Hormone integrale Mediatoren der durch Cysteinrestriktion induzierten metabolischen Veränderungen sind. Des Weiteren konnte durch die spezifische Wiederherstellung des Enzyms Cse in der Leber der Mäuse eine Normalisierung des Glutathionspiegels und der Stoffwechselparameter erreicht sowie der Gewichtsverlust verhindert werden, was die zentrale Rolle der Leber in diesem Prozess belegt.
Neben den beschriebenen molekularen und metabolischen Effekten ist auch ein signifikanter Einfluss auf die Expression zahlreicher Gene zu beobachten. Transcriptomische Analysen zeigen eine hochregulierte Expression von Genen, die an der Stressantwort, Aminosäuretransport und -stoffwechsel beteiligt sind. Gleichzeitig werden Gene, die für die Synthese von Cholesterin und Fettsäuren verantwortlich sind, herunterreguliert, was dem offenbar verringerten Bedarf nach Lipidaufbau in der Energieknappheitssituation entspricht. Die Bedeutung der CoA-Verminderung wird weiter durch die Tatsache hervorgehoben, dass Mäuse, die neben cysteinfreier Nahrung auch einen Vitamin-B5-Mangel (Pantothensäure) erleiden, nur eingeschränkt an Gewicht zulegen können, selbst nach einer Rückkehr zu Cystein-reicher Kost. Dies weist darauf hin, dass sowohl Cystein als auch Vitamin B5 gemeinsam eine notwendige Voraussetzung für eine normale CoA-Produktion und damit für einen effizienten Energiestoffwechsel sind.
Die Entdeckung der essentiellen Rolle von Cystein für die Aufrechterhaltung des Energiehaushalts und dessen Einfluss auf adipöses Gewebe eröffnet mehrere potenzielle Ansätze zur Therapie von Adipositas und verwandten Stoffwechselerkrankungen. Dabei stellt insbesondere die schnelle, reversible Gewichtsreduktion unter Cysteinrestriktion ein vielversprechendes Ziel dar. Im Gegensatz zu anderen Diätstrategien könnte die gezielte Modulation von Cysteinaufnahme oder -stoffwechsel zu effektiven, zielgerichteten und individuell anpassbaren Therapieoptionen führen. Trotz dieser vielversprechenden Erkenntnisse gilt es, einige Aspekte kritisch zu betrachten. Da Cystein unter normalen Umständen nur in begrenztem Umfang in der Nahrung vorkommt und hauptsächlich endogen erzeugt wird, bedarf es weiterer Untersuchungen, wie sich diese Mechanismen beim Menschen realistisch und sicher manipulieren lassen.