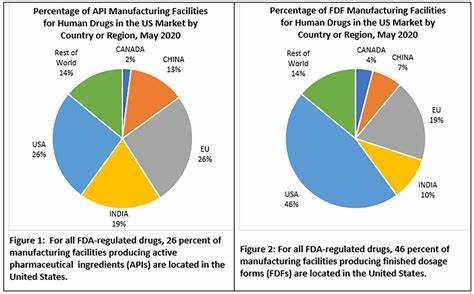
Die US-amerikanische Food and Drug Administration (FDA) hat eine bedeutende Initiative angekündigt, um die Überwachung ausländischer Herstellungsstätten von Arzneimitteln und Lebensmitteln zu verschärfen. In einem Schritt, der für die globale Pharma- und Lebensmittelindustrie weitreichende Konsequenzen haben könnte, wird die FDA die Zahl unangekündigter, überraschender Inspektionen bei ausländischen Produktionsstätten deutlich erhöhen. Dieser Wandel dient vor allem dazu, bisherige doppelte Standards zwischen inländischen Unternehmen und ausländischen Herstellern abzubauen und die Sicherheit von Arzneimitteln sowie Lebensmitteln für amerikanische Verbraucher zu stärken. Die Initiative baut auf Erfahrungen aus Pilotprogrammen in Ländern wie Indien und China auf, die bereits erfolgreich unangekündigte Besuche bei Herstellern durchgeführt haben. Die USA importieren einen Großteil ihrer Medikamente und Nahrungsmittelzutaten aus dem Ausland.
Dennoch wurden diese Produktionsstätten bislang oft vorab über Inspektionen informiert. Dies ermöglichte es den Unternehmen, die Fabriken für die Kontrolle vorzubereiten und eventuell Missstände zu kaschieren. Im Gegensatz dazu finden inspektorische Überprüfungen bei amerikanischen Firmen in der Regel ohne Vorankündigung statt. Die FDA-Kommissioner Martin Makary kritisiert diese Situation als unfair und risikobehaftet, da die Sicherheit der Verbraucher durch verzögerte oder manipulierte Inspektionen gefährdet werden kann. Die neue Strategie der FDA zielt darauf ab, dass ausländische Hersteller die gleichen Anforderungen und Kontrollen wie domestische Produzenten erfüllen müssen.
Dazu gehört auch, dass Inspektoren keine Vergünstigungen von den Unternehmen annehmen dürfen, um ihre Unabhängigkeit und Objektivität zu gewährleisten. Das bedeutet, dass Hotelübernachtungen, Transport oder andere Reisekosten nicht mehr von den geprüften Firmen getragen werden dürfen. Die FDA führt jährlich etwa 12.000 Inspektionen in den USA durch. Demgegenüber stehen circa 3.
000 Besuche im Ausland. Die ungleiche Handhabung von Vorabinformationen bei Inspektionen hat dazu geführt, dass bei ausländischen Betrieben häufiger Mängel und Verstöße festgestellt werden – mehr als doppelt so häufig wie bei amerikanischen Einrichtungen. Mit der Ausweitung unangekündigter Inspektionen sollen betrügerische Praktiken wie das Fälschen von Dokumenten oder das Verstecken von Produktionsverstößen frühzeitig erkannt und unterbunden werden. Für Unternehmen, die versuchen, Inspektionen zu verzögern, zu blockieren oder zu verweigern, sieht die FDA scharfe Maßnahmen vor. Die neue Politik ist auch vor dem Hintergrund von politischen Bestrebungen zu sehen, die Abhängigkeit von ausländischer Arzneimittelproduktion zu verringern.
Kürzlich erließ die Regierung eine Verfügung, um die Produktion von verschreibungspflichtigen Medikamenten in den USA zu fördern. Dabei sollen Antragsverfahren beschleunigt und bürokratische Hürden abgebaut werden, damit neue Anlagen schneller in Betrieb gehen können. Während sich die FDA auf strengere Kontrollen bei Importen konzentriert, wird gleichzeitig der Aufbau einer wettbewerbsfähigeren, heimischen Produktionslandschaft vorangetrieben. Für Konsumenten könnte dies zukünftig mehr Sicherheit und Verlässlichkeit bedeuten. Die Reformen reagieren auf wachsende Bedenken über die Qualität und Unversehrtheit von Lebensmitteln und Medikamenten, die in den USA auf den Markt kommen.
Die Globalisierung der Lieferketten hat zwar große Vorteile gebracht, bringt aber auch Herausforderungen hinsichtlich der Aufsicht und Qualitätssicherung mit sich. Experten und Branchenvertreter beobachten die Entwicklungen aufmerksam, da die verstärkten Inspektionen auch Auswirkungen auf Handelsbeziehungen haben könnten. Unternehmen, die Arzneimittel oder Lebensmittel exportieren, müssen eventuell mit höheren Kosten und strengeren Kontrollen rechnen. Gleichzeitig kann eine konsequentere Überwachung helfen, das Vertrauen der Verbraucher in importierte Produkte zu stärken. Zusammenfassend lässt sich sagen, dass die FDA mit der Ausweitung unangekündigter Inspektionen einen bedeutenden Schritt geht, um einheitliche Qualitätsstandards weltweit durchzusetzen.
Die amerikanische Behörde setzt verstärkt auf Prävention und Durchsetzung, um Risiken für öffentliche Gesundheit möglichst frühzeitig zu erkennen und zu minimieren. Verbraucher in den USA können somit auf eine verbesserte Kontrolle und mehr Schutz hoffen – gleichzeitig sind Hersteller global gefordert, ihre Produktionsprozesse transparenter und sicherer zu gestalten. Die Initiative verdeutlicht den hohen Stellenwert, den die FDA dem Schutz der Gesundheit beimisst und die wachsende Bedeutung einer robusten Überwachung in einer zunehmend vernetzten Weltwirtschaft.