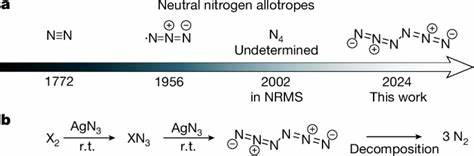
Stickstoff, als das am häufigsten vorkommende Element in der Erdatmosphäre, ist vor allem in Form des molekularen N2 bekannt – ein äußerst stabiles, inert wirkendes Molekül mit einer dreifach gebundenen Stickstoff-Stickstoff-Verbindung. Lange Zeit galt es als unmöglich, neutral molekulare Stickstoff-Allotrope jenseits von N2 herzustellen und zu isolieren, da diese als extrem instabil und reaktionsfreudig eingeschätzt wurden. Diese Einschätzung änderte sich nun grundlegend mit der erstmaligen erfolgreichen Synthese des neutralen Hexanitrogens C2h-N6, das als erste neutrale Stickstoff-Allotrop-Form nach N2 gilt. Die Entdeckung und Experimente dazu wurden kürzlich von Forschern an der Justus-Liebig-Universität Gießen veröffentlicht und haben das Verständnis polynitrogenhaltiger Verbindungen revolutioniert. Die Grundlagen für die Erforschung neuer Allotrope von Stickstoff liegen in dem hohen Energiegehalt, den diese Verbindungen theoretisch besitzen.
Im Vergleich zu Wasserstoff, Ammoniak oder Hydrazin, die bereits als Energiequellen und Raketentreibstoffe Verwendung finden, versprechen polynitrogene Verbindungen eine deutlich höhere Energiedichte. Zudem zerfallen sie bei der Zersetzung nahezu ausschließlich in molekularen Stickstoff zurück, was eine schadstofffreie, umweltfreundliche Reaktion suggeriert. Doch der größte Stolperstein lag bisher in der Synthese solcher stabiler neutraler Stickstoffmoleküle, denn ihre Tendenz, spontan in das stabile N2 zu zerfallen, ist enorm stark. Ausgehend von früheren Studien, in denen lediglich anionische oder kationische Formen von polynitrogentypischen Verbindungen in Feststoff- oder Hochdruckphasen isoliert werden konnten, gelang es Forschern jetzt, C2h-symmetrisches Hexanitrogen als neutrales Molekül im Labor zu erzeugen. Die Vorgehensweise basierte auf der Gasphasenreaktion von Chlor- oder Bromgas mit Silberazid (AgN3).
Die Reaktion fand bei Raumtemperatur unter reduziertem Druck statt, gefolgt von einer schnellen Einfrierung der Produkte in einem Argon-Matrix bei nur 10 Kelvin. Dort wurde das N6-Molekül mittels Infrarot- und UV-Vis-Spektroskopie sowie ^15N-Isotopenmarkierung eindeutig nachgewiesen. Zusätzlich konnte N6 als reines Film bei Temperaturen von 77 Kelvin hergestellt und stabil gehalten werden, was seine Stabilität über den kurzzeitigen analytischen Nachweis hinaus demonstriert. Die Struktur des hexanitrogens Moleküls ist keinesfalls trivial und unterscheidet sich deutlich von den bekannten Formen wie z.B.
dem linearen Azidradikal (•N3). Stattdessen ist C2h-N6 als ein acyclisches Molekül mit zwei N3-Moitäten beschrieben, die durch eine zentrale N–N-Einfachbindung verbunden sind. Berechnungen ergaben N–N-Bindungslängen, die dem Charakter von Doppelbindungen entsprechen, und bestätigten die elektronische Neutralität der terminalen Stickstoffatome. Besonders interessant sind die theoretisch berechneten Energiebahnen, die eine vergleichsweise hohe Dissociationsbarriere für den Zerfall in drei molekulare Stickstoffeinheiten zeigen. Dadurch besitzt N6 trotz seiner erwarteten Reaktivität eine kinetische Stabilität, die bislang bei neutralen Stickstoff-Allotropen nicht beobachtet wurde.
Die Synthese von N6 beruht auf der für Silberazid charakteristischen Reaktivität gegenüber Halogenverbindungen in der Gasphase. Silberazid wurde dabei auf der Innenseite von Quarzröhren oder U-förmigen Gefäßen in geringer Menge aufgebracht und anschließend durch Chlor- oder Bromgas bei reduziertem Druck durchströmt. Die Reaktionsprodukte wurden unmittelbar anschließend mit Argon co-kondensiert und in einer Matrix bei extrem niedrigen Temperaturen eingefroren. Die entstehenden Moleküle konnten so im Detail mittels IR- und UV-Vis-Spektroskopie untersucht werden. Das Auffinden spezifischer Schwingungsfrequenzen und das Verhalten unter Lichtbestrahlung erlaubten den Forschern eine eindeutige Identifikation von N6.
Ergänzende Isotopenmarkierungs-Experimente mit ^15N bestätigten zudem das Vorhandensein der beiden N3-Moitäten. Die stabile Existenz von N6 in einer reinen, kompakten Schicht bei flüssigem Stickstoff unterstreicht die neuartige kinetische und teils thermodynamische Stabilität, die dieser bisher unbekannten Stickstoff-Allotropform innewohnt. So kann N6 als Filmmaterial einige Minuten bei 77 Kelvin überstehen, ein Zeitraum, der für zukünftige Untersuchungen und mögliche Anwendungen entscheidend ist. Ein weiterer Meilenstein der Forschungen bildet die theoretische Modellierung der elektronischen Struktur und Reaktionsprofile. Hochwertige Berechnungsmethoden auf CCSD(T)-Niveau zeigten, dass nur die trans-C2h-Konformation von N6 ein echtes energetisches Minimum darstellt, während andere mögliche Isomere instabil sind.
Die elektronischen Ladungsverteilungen hinsichtlich natürlicher Bindungsorbitale unterstützten dabei die Beschreibung eines frisch entdeckten kohärenten Moleküls mit ausgewogenem Ladungsprofil. Die Visualisierung der Elektronendichte, insbesondere durch Laplacian- und Elektronenlokalisierungsfunktionen, identifizierte die kritischen Bindungen und mögliche Zerfallswege. Besonders die vergleichsweise hohe Aktivierungsbarriere für den Zerfall in drei N2-Moleküle von etwa 14,8 kcal/mol erklärt, warum N6 länger als nur Bruchteile von Sekunden existieren kann. Auch quantenmechanische Tunneleffekte scheinen für den Zerfall von N6 eine deutlich geringere Rolle zu spielen als etwa bei anderen theoretisch vorgeschlagenen Allotropen wie dem aromatischen Hexazin. Dies macht N6 erstmals zu einem erreichbaren neutralen Stickstoff-Molekül mit einem messbaren, wenn auch begrenzten Haltbarkeitszeitraum bei Raum- bis Tieftemperaturen.
Neben seinen fundamentalen wissenschaftlichen Relevanz weist N6 als energetisches Material ein enormes Potential auf. Die Berechnungen deuten darauf hin, dass die Zersetzung von N6 mit einer Energiefreisetzung von über 185 kcal/mol ein Vielfaches der Energie von gängigen Sprengstoffen wie TNT oder HMX freisetzt, und dies bei der ausschließlichen Rückbildung zu gasförmigem Stickstoff. Die kinetische Stabilität, kombiniert mit der hohen Energetik und dem sauberen Abbauprodukt, macht N6 zu einem bedeutenden Kandidaten für zukünftige nachhaltige Energiespeicher und Hochleistungsenergiematerialien. Damit steht N6 stellvertretend für eine neue Generation von molekularen Stickstoff-Allotropen, die das Potential besitzen, alte Vorstellungen von stabiler Stickstoffchemie infrage zu stellen. Die Syntheseweg zeichnet sich durch vergleichsweise geringe technische Anforderungen aus, da die Reaktion bei Raumtemperatur und moderatem Druck durchführbar ist.
Die Kombination von experimenteller Matrixtechnologie und präziser computergestützter Analyse setzte somit einen wichtigen Impuls für die praktische Erforschung bisher hypothetischer polynitrogener Molekülformen. Zusammenfassend markiert die erfolgreiche Herstellung und Charakterisierung von Hexanitrogen C2h-N6 einen technischen und wissenschaftlichen Durchbruch mit weitreichenden Konsequenzen. Von der Grundlagenchemie über neue Energiekonzepte bis hin zur Materialwissenschaft eröffnet das neue Molekül neue Forschungsfelder und Anwendungsmöglichkeiten. In Zukunft können weitere Studien zur Stabilitätsverbesserung, Handhabung und potentiellen Nutzung in umweltfreundlichen Hochenergieanwendungen folgen. Die Arbeiten zeigen eindrucksvoll, dass vorab als unerreichbar geltende neutral-molekulare Stickstoff-Allotrope nun endlich experimentell zugänglich sind.
Dies ist ein Schritt in Richtung nachhaltigerer Chemie mit molekularen Energieträgern, die eine grüne Alternative zu fossilen Brennstoffen und umweltschädlichen Energiespeichern darstellen können. Die Kombination aus innovativer Gasphasenreaktion, cleverer Matrixisolierung und moderner Spektroskopie mit computergestütztem Design ist ein Musterbeispiel für interdisziplinäre Forschung mit globaler Bedeutung.