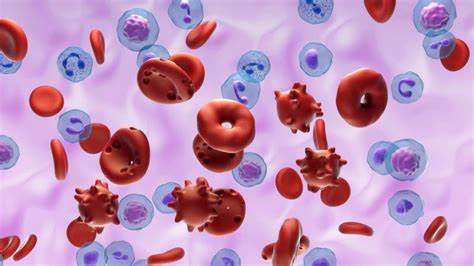
Blutgerinnung ist schon lange ein fundamentales Thema in der Medizin und Biologie, insbesondere im Zusammenhang mit der Behandlung von Herzkrankheiten und Schlaganfällen. Doch trotz jahrzehntelanger Forschung haben Wissenschaftler nun eine völlig neue und überraschende Entdeckung gemacht, die das Verständnis von vaskulären Prozessen revolutionieren könnte. Forscherteams aus Australien und New York haben einen bislang unbekannten biologischen Mechanismus identifiziert, der bei Sauerstoffmangel in Geweben eine zentrale Rolle spielt und das Gefäßsystem auf eine Art beeinflusst, die bisher nicht verstanden wurde. Diese Entdeckung verspricht neue Behandlungsmöglichkeiten für lebensbedrohliche Erkrankungen und öffnet ein neues Kapitel in der Gefäßbiologie. Im Fokus steht nicht mehr die herkömmliche Blutgerinnung durch Plättchen und Fibrin, sondern ein Prozess, der mit dem Zerplatzen roter Blutkörperchen zusammenhängt und zur Verstopfung kleinster Blutgefäße führt.
Die Mikrovaskulatur, also das Netzwerk der kleinsten Blutgefäße im Körper, ist entscheidend für die Versorgung von Organen und Geweben mit Sauerstoff und Nährstoffen. Gerät diese Versorgung ins Stocken, kann das schwerwiegende Folgen haben – von Gewebeschäden bis hin zum Organversagen. Gerade bei Herzinfarkten, Schlaganfällen oder auch schweren COVID-19-Infektionen wurde die Mikrogefäßfunktion als ein kritischer Faktor erkannt. Bislang ging die Forschung davon aus, dass Blutgerinnsel aufgrund von Plättchenaggregation und Fibrinnetzen die Ursache für die Verstopfungen kleinster Gefäße sind. Dieser konventionelle Gerinnungsmechanismus sorgt dafür, dass bei Verletzungen die Blutung gestoppt wird, indem ein stabiler Pfropf gebildet wird.
Die neue Untersuchung wirft diesen Gedanken jedoch über Bord. Sie offenbart, dass in kritischen Situationen das eigentliche Problem durch das Platzen roter Blutkörperchen entsteht. Diese Hämolyse setzt Membranen und proteinhaltige Materialien frei, die eine Art biologischen Klebstoff bilden. Sichtbar wird eine klebrige Substanz, die sich an beschädigten Gefäßwänden ablagert und die Mikrozirkulation nachhaltig blockiert. Der leitende Forscher, Professor Shaun Jackson, betont, dass es sich um einen völlig neuen Blutgerinnungsmechanismus handelt, der unabhängig von bekannten Prozessen mit Plättchen oder Fibrin ist.
Diese Erkenntnis hat nicht nur grundlegende wissenschaftliche Bedeutung, sondern könnte auch erhebliche Auswirkungen auf die Klinische Praxis haben. Insbesondere bei Patienten mit schwerem COVID-19-Verlauf beobachteten die Forscher massiv geschädigte Endothelzellen, welche die Innenschicht der Blutgefäße bilden. Die blutzirkulierenden roten Blutkörperchen platzen und entlassen ihr inneres Material, das sich in den Mikrovaskularen der Lunge, des Herzens, der Nieren und der Leber ablagert. Dieses Phänomen erklärt, warum herkömmliche Gerinnungshemmer bei der Behandlung von COVID-19 Mikrogefäßproblemen oft nur begrenzt wirksam sind. Interessanterweise bestätigt die Forschung, dass dieses Muster der Gefäßblockade nicht nur bei COVID-19 auftritt, sondern auch in Modellen von Herzinfarkt, Schlaganfall und Darmischämie nachweisbar ist.
Die Folgen dieses neu entdeckten Mechanismus reichen damit weit über eine einzelne Erkrankung hinaus und werfen umfassende Fragen zur Pathophysiologie vieler kritischer Zustände auf. Die Erkenntnis bringt neue Hoffnung für therapeutische Ansätze. Anstatt Blutgerinnsel einzeln durch Hemmung von Plättchen oder Fibrin zu bekämpfen, schlagen die Wissenschaftler vor, den Prozess der Endothelzellschädigung frühzeitig zu verhindern oder die Hämolyse der roten Blutkörperchen gezielt zu blockieren. Wenn es gelingt, diesen „glue-like“ Effekt der Zellmembranen aufzuhalten, könnte die Durchblutung von Mikrogefäßen bewahrt und somit Organschäden reduziert werden. Dies würde nicht nur Patienten mit COVID-19, sondern auch vielen anderen Patienten mit kritischen Krankheitsverläufen zugutekommen.
Außerdem zeigt die Entdeckung noch einmal die Komplexität und Raffinesse biologischer Systeme auf. Die traditionellen Methoden der Gerinnungsanalyse und -therapie müssen daher neu überdacht und erweitert werden, um die Vielfalt der Prozesse in der Mikrozirkulation zu erfassen. Auch die Rolle der roten Blutkörperchen, lange Zeit nur als Sauerstofftransporter betrachtet, erhält mit dieser Studie eine ganz neue Dimension. In der Summe stellen die Ergebnisse eine enorme Chance dar, unser Verständnis von vaskulären Erkrankungen zu vertiefen und innovative Behandlungskonzepte zu entwickeln. Langfristig könnten neue Medikamente entwickelt werden, die gezielt die Schädigung von Endothelzellen verhindern oder die Ablagerung der membranösen Substanzen neutralisieren.
Damit eröffnen sich Potenziale, die Lebensqualität von Patienten mit Herzinfarkt, Schlaganfall, mehreren Organfunktionsstörungen und anderen kritischen Erkrankungen signifikant zu verbessern. Die Studie erschien in der renommierten Fachzeitschrift Nature und steht exemplarisch für interdisziplinäre Forschung, die klinische Beobachtungen mit molekularbiologischen Erkenntnissen verbindet. Neben den unmittelbaren medizinischen Auswirkungen bedeutet die Entdeckung auch einen Paradigmenwechsel in der Gefäßbiologie. Die Mechanismen, die Mikrogefäße im Körper funktionsfähig halten oder zum Versagen bringen, sind komplexer als gedacht und erfordern neue Forschungsansätze. Insgesamt lässt sich festhalten, dass die Identifikation eines neuen Blutgerinnungsmechanismus, der auf wirksame Weise die Mikrogefäße verstopft, ein bedeutender Fortschritt in der biomedizinischen Wissenschaft darstellt.
Er erweitert das Wissen über die Pathogenese von Herz-Kreislauf-Erkrankungen, Entzündungsprozessen und Organversagen. Darüber hinaus weist auch die Rolle der Endothelzellgesundheit als mögliche therapeutische Zielstruktur einen vielversprechenden Weg in der klinischen Forschung. Die Erkenntnisse zeigen, wie wichtig kontinuierliche Forschung ist, um die Mechanismen lebensbedrohlicher Krankheiten besser zu verstehen und dadurch wirksame Therapien entwickeln zu können. In einer Zeit, in der Herzinfarkte und Schlaganfälle zu den häufigsten Todesursachen zählen, öffnet die Entdeckung neue Türen und könnte zukünftig Millionen von Patienten helfen, indem sie innovative Behandlungsmöglichkeiten erlaubt. Es bleibt spannend zu beobachten, wie sich diese Erkenntnisse klinisch umsetzen lassen und welche neuen Medikamente und Therapien daraus entstehen.
Die Zukunft der Gefäßmedizin steht ganz im Zeichen dieser faszinierenden neuen Entdeckung und markiert einen Wendepunkt im Kampf gegen vaskuläre Erkrankungen.