Die Erforschung biologischer Prozesse in lebenden Organismen erfordert hochmoderne bildgebende Verfahren, die präzise, schnell und minimal invasiv sind. In den letzten Jahren hat sich die Hochgeschwindigkeits-Fluoreszenz-Lichtfeld-Tomographie als bahnbrechende Technologie etabliert, die es ermöglicht, dreidimensionale Bilder ganzer frei beweglicher Organismen in Echtzeit zu erfassen. Diese Methode verbindet die Vorteile der Fluoreszenzbildgebung mit den komplexen Aufnahme- und Rekonstruktionsprinzipien der Lichtfeldtechnik und eröffnet neue Horizonte in der Lebenswissenschaft. Die Fluoreszenzbildgebung basiert darauf, dass spezifische biomolekulare Marker durch Anregung mit geeigneter Wellenlänge Licht emittieren. Diese Emission kann sensibilisiert und präzise detektiert werden, wodurch spezifische Strukturen oder physiologische Prozesse sichtbar gemacht werden.
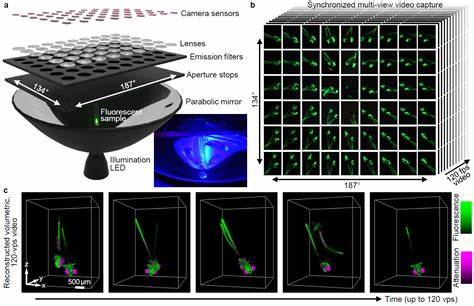
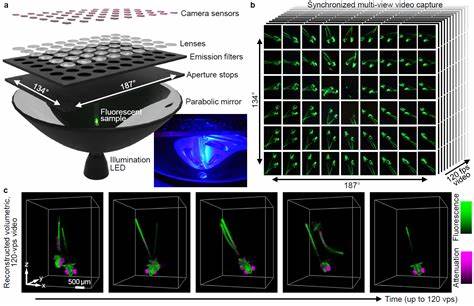
Allerdings ist es eine Herausforderung, bei lebenden Organismen nicht nur qualitative, sondern auch quantitative 3D-Daten zu generieren – vor allem, wenn diese sich frei und ungehindert bewegen. Traditionelle bildgebende Verfahren wie konfokale Mikroskopie oder Zwei-Photonen-Mikroskopie bieten zwar hohe Auflösung, sind jedoch oft durch langsame Aufnahmezeiten und den Bedarf an fixierten oder eingeschränkten Proben limitiert. Hier setzt die Hochgeschwindigkeits-Fluoreszenz-Lichtfeld-Tomographie an. Das Verfahren nutzt die Fähigkeit von Lichtfeldkameras, nicht nur die zweidimensionale Lichtintensität zu erfassen, sondern auch die Richtung des Lichts. Dadurch kann das dreidimensionale Volumen eines Objekts mit nur einer Aufnahme rekonstruiert werden, was die Geschwindigkeit der Datenerhebung dramatisch erhöht.
In Kombination mit fluoreszenzmarkierten Organismen bedeutet dies, dass man hochauflösende 3D-Bilder von biologischen Vorgängen erhalten kann, während sich das Medientier frei bewegt. Die gesamte Prozedur ist schnell genug, um Dynamiken in Echtzeit abzubilden, was für Studien zur neuronalen Aktivität, zum Verhalten und zur Physiologie von entscheidender Bedeutung ist. Die Herausforderung bestand lange darin, dieses Verfahren in einem Umfang anzuwenden, der komplette Organismen erlaubt. Kleinmodellorganismen wie der Fadenwurm Caenorhabditis elegans oder Zebrafischlarven sind ideale Kandidaten, um neuronale Netzwerke und Bewegungsmuster ganzheitlich zu erforschen. Durch genetische Markierung selektiver Zelltypen mit fluoreszenten Proteinen wird die selektive Sichtbarkeit bestimmter Strukturen gewährleistet.
Die Lichtfeldtechnik erfasst diese Signale in vollem Volumen, ohne dass die Tiere für die Dauer der Aufnahme fixiert oder eingeschränkt werden müssen. Das erlaubt faszinierende Beobachtungen von Interaktionen, Umweltwahrnehmung und motorischer Steuerung in einem natürlichen Bewegungsablauf. Technisch basiert die Lichtfeld-Tomographie typisch auf einem Array von Mikroobjektiven oder speziellen Kamerasystemen, die Lichtstrahlen in verschiedene Winkel aufnehmen. Ein komplexer Algorithmus verarbeitet die aufgenommenen Daten und errechnet daraus das 3D-Abbild des fluoreszierenden Objekts. Die Echtzeitfähigkeit resultiert aus der Kombination moderner Hochgeschwindigkeitskameras und optimierter Rechenverfahren, die oft GPU-beschleunigt sind.
Die Anwendungen sind breit gefächert. In der Neurobiologie ermöglichen solche Bildgebungstechniken das Messen neuronaler Aktivität während der Bewegung, was neue Einsichten in das Verständnis von Sensorik, Signalverarbeitung und motorischer Kontrolle erlaubt. Aufgrund der hohen zeitlichen und räumlichen Auflösung können Forscher erstmals direkte Korrelationen zwischen neuronaler Dynamik und Verhaltensmustern ziehen. Ebenso profitieren Entwicklungsbiologen von der Möglichkeit, Embryonalentwicklungen ohne Fixierung und in ihrem natürlichen Bewegungsrahmen zu analysieren. Selbst in der Pharmakologie bieten sich neue Ansätze an, Tiere mit Wirkstoffen zu konfrontieren und gleichzeitig deren physiologische Reaktion dreidimensional und in Echtzeit zu überprüfen.
Dennoch gibt es Herausforderungen, die kontinuierlich adressiert werden müssen. Die Datenmenge, die bei diesen schnellen 3D-Aufnahmen anfällt, erfordert leistungsfähige Speicher- und Verarbeitungslösungen. Ebenso stellt die Lichtstreuung in biologischem Gewebe eine limitierende Größe hinsichtlich der Eindringtiefe und Bildqualität dar. Vielversprechende Ansätze wie die Kombination mit adaptiver Optik oder die Nutzung neuer fluoreszenter Marker verbessern jedoch stetig die Leistungsfähigkeit und Auflösung des Systems. Zusammenfassend lässt sich sagen, dass die Hochgeschwindigkeits-Fluoreszenz-Lichtfeld-Tomographie eine revolutionäre Technologie ist, die das Potenzial hat, die Erforschung dynamischer biologischer Prozesse auf zellulärer und organismischer Ebene grundlegend zu verändern.
Indem sie hochauflösende und schnelle 3D-Aufnahmen ermöglicht, fördert sie ein tieferes Verständnis der komplexen Wechselwirkungen in lebenden Systemen. Mit weiteren technischen Innovationen und breiterer Anwendung wird diese Methode in Zukunft eine zentrale Rolle in der biomedizinischen Forschung spielen und dazu beitragen, neue Therapien und Ansätze zur Behandlung von Krankheiten zu entwickeln.