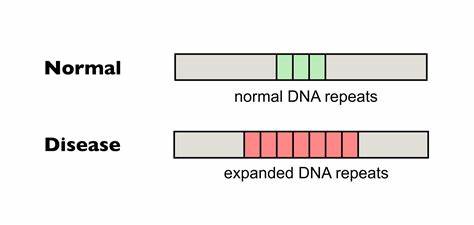
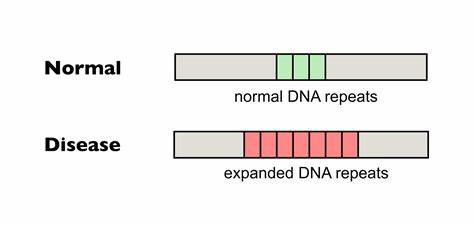
Huntington ist eine genetisch bedingte neurodegenerative Erkrankung, die durch die Expansion bestimmter trinukleotidischer Repeat-Sequenzen im Huntingtin-Gen (HTT) ausgelöst wird. Dieses Phänomen, bei dem sich CAG-Repeatsequenzen im Genom verlängern, führt unweigerlich zu einer fehlerhaften Produktion eines toxischen Proteins, das Nervenzellen schädigt und zum frühzeitigen Verlust motorischer, kognitiver und psychischer Funktionen führt. Die Intensität und das Auftreten der Krankheit korrelieren dabei eng mit der Länge der CAG-Repeats. Lange Repeats begünstigen dabei eine instabile genomische Situation, die sich vor allem durch somatische Expansionen – also der Verlängerung der Repeat-Sequenzen in Körperzellen nach der Geburt – manifestiert. Neue wissenschaftliche Erkenntnisse zeigen jedoch, dass gezieltes Editing dieser Repeats mittels moderner biotechnologischer Methoden wie dem sogenannten Base Editing vielversprechende Ansätze liefern könnte, um somatische Repeat-Expansionen zu reduzieren oder sogar rückgängig zu machen.
Somatische Repeat-Expansionen: Der Schlüssel zur Progression Die genetische Grundlage von Huntington beruht auf der Mutation, bei der an einer bestimmten Stelle im HTT-Gen eine Reihe von CAG-Tripletts, welche für die Aminosäure Glutamin codieren, über ein Normalmaß hinaus verlängert ist. Ein gesunder Mensch trägt meist unter 35 Wiederholungen, wohingegen Patienten mit Huntington oft 36 oder mehr besitzen. Diese längeren Repeat-Sequenzen sind nicht stabil, sondern neigen dazu, sich im Laufe des Lebens in verschiedenen Geweben, besonders im Gehirn, weiter zu verlängern. Die somatischen Expansionen führen nicht nur zu einem größeren Funktionsverlust der betreffenden Nervenzellen, sondern korrelieren auch mit dem Verlauf und dem Alter bei Ausbruch der Krankheit. Längere und reinartige (ununterbrochene) Repeats zeigen eine höhere Instabilität.
Besonders in Neuronen beobachtet man, dass sich die Repeat-Regions längenweise unkontrolliert erweitern, was erst spät im Krankheitsgeschehen zu sichtbaren Problemen führt. Somit stellt die Verhinderung oder Umkehr dieser somatischen Expansionen eine entscheidende therapeutische Zielsetzung dar. Die Bedeutung von Interruptions – Unterbrechungen in der Repeats Interessanterweise weisen Studien darauf hin, dass eine Unterbrechung der CAG-Sequenzen durch einzelne Nucleotidvarianten, sogenannte Interruptions, die Repeats stabilisieren und die Menge somatischer Expansionen reduzieren. Beispielsweise führt die Insertion von CAA-Codons innerhalb langer CAG-Trakte zu einer gleichen Aminosäuresequenz (Glutamin bleibt Glutamin), erschwert allerdings die Ausdehnung und Neubildung instabiler Sekundärstrukturen in der DNA. Patienten mit solchen Interruptions zeigen häufig spätere Krankheitsausbrüche und milder verlaufende Symptome.
Dies untermauert die Hypothese, dass gezielte Einbringen dieser Interruptions vorteilhaft sein kann, indem die progressiven Erweiterungen der Repeat-Sequenzen effektiv gebremst werden. Base Editing: Präzise Werkzeugtechnologie für die Genommodifikation Diese neuen, natürlichen Befunde bieten eine hervorragende Grundlage für Entwicklungsarbeiten mit der CRISPR-basierenden Base Editing-Technologie. Im Gegensatz zu klassischen CRISPR/Cas9-Systemen, die Doppelstrangbrüche erzeugen, können Base Editor einzelne Nukleotide gezielt umwandeln – bei Huntington etwa Cytosin zu Thymin oder Adenin zu Guanin – ohne das Genom schädlich zu durchschneiden. Das erlaubt das punktgenaue Einfügen von Interruptions in die CAG-Tracts bei HTT und die gleichzeitige Auslöschung oder Reduktion der somatischen Expansionen. Kürzlich wurden innovative Cytosin- und Adenin-Base Editor entwickelt, die mit AAV9-Vektoren effizient in Modelle wie humane Zellen oder transgene Mäuse eingebracht wurden.
Im Fall von Huntington wurde durch gezielte Cytosin-Base Editing an den CAG-Repeats eine Synonymcodierung (CAG zu CAA) etabliert, die die Anzahl reiner CAG-Sequenzen verringert. Die Intervention zeigte sowohl im vitro in Patientenfibroblasten als auch in vivo in Htt.Q111-Mausmodellen eine signifikante Verringerung der somatischen Expansion, verbunden mit stabileren Repeat-Längen und reduzierten neurodegenerativen Markern. Vielversprechende Ergebnisse in Patientenzellen und Tiermodellen In kultivierten Fibroblasten von Huntington-Patienten konnten durch die Einbringung von Interruptions mittels Base Editing bis zu 80 % der sonst reinen CAG-Trakte erfolgreich modifiziert werden. Diese Änderungen waren stabil und zeigten im zeitlichen Verlauf der Zellkultur eine klare Reduktion der somatischen Expansion.
Ergänzend wurden in transgenen Mäusen durchschnittlich 30 % der HTT-Repeats mit Interruptions versehen, was zu einer messbaren Reduktion der somatischen Expansionsrate, besonders in Gehirnbereichen wie dem Striatum führte. Diese Effekte bestanden über Monate hinweg und zeigten keine unerwünschten Nebenwirkungen oder erhöhte Off-Target Mutationen in entscheidenden Genregionen. Die molekularen Mechanismen hinter dieser Stabilisierung lassen sich auf die verminderte Bildung außerordentlicher DNA-Strukturen zurückführen, die bei reinen langen Repeats entstehen und für fehlerhafte DNA-Reparaturprozesse verantwortlich sind. Interruptions scheinen diese Strukturen zu unterbrechen und so die DNA-Stabilität zu erhöhen. Therapeutische Perspektiven und Herausforderungen Die Nutzbarmachung von Base Editing zur Behandlung von Huntington eröffnet ein neues therapeutisches Fenster.
Anders als Heilmethoden, die auf Symptomkontrolle setzen, spricht Base Editing die molekulare Ursache an und kann potenziell das Fortschreiten der Erkrankung verlangsamen oder sogar frühzeitig verhindern. Ein besonderer Vorteil liegt darin, dass Codon-Interruptions die Proteinsequenz nicht verändern, somit das Risiko unerwünschter Effekte minimiert wird. Dennoch bestehen Herausforderungen. Die effiziente und sichere Lieferung der Base Editing-Komponenten in die relevanten Zelltypen des Zentralnervensystems bleibt anspruchsvoll. Langzeitstudien und umfassende Off-Target-Analysen sind notwendig, bevor klinische Anwendungen beginnen können.