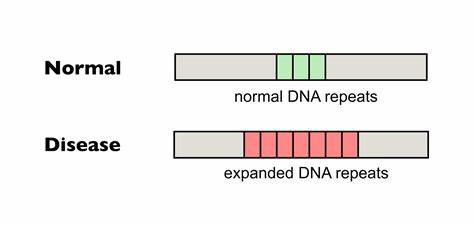
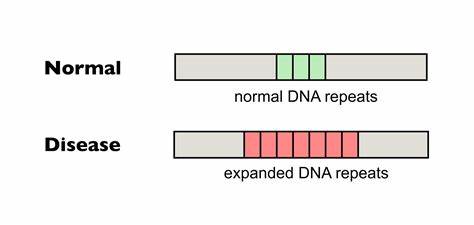
Die Huntington-Krankheit (HD) zählt zu den bekanntesten erblichen neurodegenerativen Erkrankungen, die durch die Expansion von trinukleotidischen Wiederholungen im Huntingtin (HTT)-Gen ausgelöst wird. Diese CAG-Wiederholungen, die sich im Gen abschnittsweise vermehren können, führen dazu, dass ein toxisches Polyglutamin-Protein entsteht, welches Nervenzellen schädigt und zum fortschreitenden Verlust motorischer und kognitiver Funktionen führt. Ein zentrales Merkmal der HD ist die Instabilität dieser CAG-Wiederholungen, die im Verlauf des Lebens in somatischen Zellen weiter expandieren können, was den Krankheitsverlauf verschärft und den Ausbruch beschleunigt. Die Herausforderung besteht darin, diese somatischen Wiederholungsexpansionen zu hemmen oder zu stabilisieren, um die Krankheit progressiv zu verlangsamen oder gar aufzuhalten. In den letzten Jahren haben molekulare Fortschritte im Bereich der Genom-Editierung neue therapeutische Perspektiven eröffnet.
Besonderes Interesse gilt sogenannten Base-Editoren, die gezielte chemische Veränderungen einzelner Nukleotide ohne das Erzeugen von Doppelstrangbrüchen bewirken. Diese Technik ermöglicht eine äußerst präzise Modifikation der DNA-Sequenz und bietet insbesondere bei wiederholenden Sequenzen wie den CAG-Trinukleotiden vielversprechende Ansätze zur Intervention. Aktuelle Studien zeigen, dass durch den Einsatz von cytosin- und adenine-basierten Editoren gezielt sogenannte Interruptions verbessert werden können. Dabei werden natürliche Unterbrechungen in den Wiederholungssequenzen eingeführt – aus CAG wird beispielsweise CAA, welches zwar die Aminosäure Glutamin codiert, allerdings die Struktur und Stabilität der Wiederholung positiv beeinflusst. Solche Interruptions sind in Populationen bereits natürlich vorkommend und werden mit einer geringeren Neigung zu somatischen Expansionen sowie einem späteren Krankheitsbeginn in Verbindung gebracht.
Experimente an menschlichen Patientenzellen sowie in vivo an murinen Modellen der Huntington-Krankheit bestätigen die Effektivität dieser Methode. Durch die gezielte Einführung von Basenänderungen in den HTT-Wiederholungstrakten wurde eine signifikante Reduktion der somatischen Expansionen beobachtet. Patientenzelllinien, die durch mRNA-basierte Elektroporation mit Base-Editoren behandelt wurden, zeigten eine Verringerung der CAG-Repeats über mehrere Zellgenerationszyklen hinweg. In HD-Mausmodellen führte die Verabreichung der Editoren mittels Adeno-assoziierter Viren (AAV) in den Zentralnervensystembereichen zu einer nachhaltigen Stabilisierung und sogar Verkürzung der pathogenen Wiederholungstrakte. Im Detail zeigte sich, dass die Anzahl der Interruptions mit der Effizienz der Injektion und der Expression der Base-Editoren korreliert.
Dabei werden mehrfach Hinterfragungen zur Limitation von Off-Target-Effekten durch sogenannte CIRCLE-Seq-Analysen adressiert. Diese umfassen genomeweite Suchverfahren nach potenziellen unerwünschten Editierungen, die allerdings überwiegend in nicht-kodierenden Bereichen auftreten und selten zu funktionellen Veränderungen führen. Das therapeutische Potenzial dieser Technik ist enorm. Indem somatische Wiederholungsexpansionen schon bei frühen Stadien der Erkrankung gebremst werden können, eröffnet sich die Möglichkeit, den Verlauf der Huntington-Krankheit zu verzögern und damit Lebensqualität und Funktionalität der Patienten positiv zu beeinflussen. Gerade aufgrund der bislang fehlenden kurativen Therapien für Polyglutamin-Erkrankungen ist die Base-Editing-Methode ein vielversprechender Kandidat für zukünftige klinische Anwendungen.
Doch trotz der Erfolge stehen auch Herausforderungen im Raum. Die langfristige Sicherheit, die Kontrolle über die Expression der Editoren im menschlichen Körper und die effiziente Verteilung in relevanten Geweben sind Gegenstand aktueller Forschung. Zudem gilt es, individuelle genetische Unterschiede und mögliche Immunreaktionen zu berücksichtigen. Fortschritte in der Vektorentwicklung und der gezielten Auslieferung könnten diese Hürden überwinden helfen. Neben Huntington eröffnet die Base-Editing-Technologie viele weitere Anwendungsmöglichkeiten für andere Erkrankungen mit genetischer Grundlage, insbesondere bei weiteren trinukleotidischen Wiederholungskrankheiten wie Friedreich-Ataxie oder verschiedenen Spinocerebellären Ataxien.
Die universelle Strategie, pathogene Repeat-Tracts durch Einfügen natürlicher Interruptions zu stabilisieren, hat das Potenzial, das therapeutische Spektrum für diese bisher unheilbaren Krankheiten wesentlich zu erweitern. In der Kombination aus molekularer Genetik, Biotechnologie und klinischer Translation zeigt sich, wie präzise Genomeditierung zu einem mächtigen Werkzeug für die Therapie bisher schwer behandelbarer neurologischer Erkrankungen werden kann. Die Verringerung somatischer Repeat-Expansionen stellt dabei einen entscheidenden Schritt dar, der nicht nur symptomatisch wirkt, sondern direkt in die Ursache der Huntington-Krankheit eingreift. Die nächsten Jahre werden zeigen, wie diese vielversprechenden Labordaten in klinische Studien und schließlich in reale Therapien übersetzt werden können. Die interdisziplinäre Zusammenarbeit zwischen Wissenschaftlern, Klinikern und Pharmaindustrie wird maßgeblich den Erfolg und die Akzeptanz dieser Techniken in der Patientenversorgung bestimmen.
Abschließend lässt sich sagen, dass das Genom-Editing mittels Base-Editoren eine revolutionäre Entwicklung im Kampf gegen die Huntington-Krankheit darstellt. Die Möglichkeit, somatische Repeat-Expansionen gezielt zu reduzieren, könnte das Verständnis und die Behandlung genetisch bedingter neurodegenerativer Erkrankungen grundlegend verändern und neue Hoffnungen für Patienten und ihre Familien wecken.