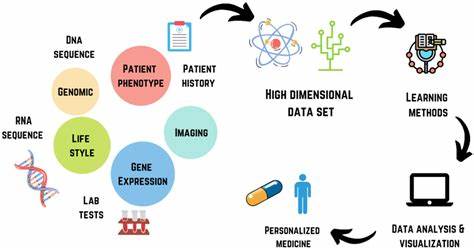
Die Einbindung von Künstlicher Intelligenz (KI) in die Arzneimittelentwicklung hat sich in den letzten Jahren rasant weiterentwickelt. Im Jahr 2025 zeigt sich eine zunehmende Verbreitung und Akzeptanz von KI-Technologien innerhalb der Wirkstoffforschung, jedoch bleiben gewisse Herausforderungen, die den breiteren Einsatz bislang einschränken. Die medizintechnische und pharmazeutische Industrie erlebt derzeit einen Wandel, der von Pragmatismus und realitätsnahen Anwendungen geprägt ist – weg von überzogener Euphorie und skeptischer Zurückhaltung früherer Jahre hin zu konkreten Lösungsansätzen und strukturierter Implementierung. Dies ist besonders auf Veranstaltungen wie die Bio-IT World 2025 in Boston zu beobachten, die seit jeher als Barometer für technologische Entwicklungen in diesem Bereich dient. Ein zentrales Thema in der aktuellen Diskussion ist die Demokratisierung der KI.
Längst sind die mächtigen Modelle und Algorithmen nicht mehr ausschließlich großen Konzernen oder spezialisierten Forschungseinrichtungen vorbehalten. Die Erstellung und Nutzung von KI-Modellen gewinnt zunehmend an Breitenwirkung, wodurch immer mehr Teams in der Wirkstoffforschung Zugang zu diesen innovativen Werkzeugen erhalten. Dies beschleunigt nicht nur interne Prozesse, sondern fördert auch die Kollaboration zwischen Unternehmen, akademischen Instituten und kleineren Start-ups. In diesem Zusammenhang spielt die Entwicklung von benutzerfreundlichen Plattformen und Anwendungen eine Schlüsselrolle. So bietet Chemaxon beispielsweise mit seinen Produkten wie dem „Design Hub“ oder „Marvin“ intuitive Schnittstellen, die insbesondere Chemikern in der Wirkstoffentwicklung helfen, KI gestützte Analysen und Designs umzusetzen.
Parallel dazu gewinnt die Etablierung zentraler Unternehmensrichtlinien für die Nutzung von KI zunehmend an Bedeutung. Im Gegensatz zu den „Wildwest“-Zeiten zu Beginn der KI-Integration ist heute eine sorgfältige Regulierung und Überwachung der Algorithmen unabdingbar. Datenschutz- und Sicherheitsfragen sind in der pharmazeutischen Industrie besonders sensibel, da viele eingesetzte Modelle mit vertraulichen Daten arbeiten. Unternehmen setzen daher vermehrt auf On-Premise-Deployments, um sensible Informationen ausschließlich innerhalb der eigenen IT-Infrastruktur zu verarbeiten. Außerdem werden Risikoprofile erstellt, die genau festlegen, in welchem Umfang und für welche Entscheidungen KI-Systeme mitwirken dürfen.
Gerade bei hochsensiblen oder kritischen Aufgaben erfolgt eine Validierung der verwendeten Modelle, um potenzielle Fehlentscheidungen zu minimieren. Ein weiteres wesentliches Kriterium für den erfolgreichen Einsatz von KI in der Wirkstoffforschung ist die Transparenz der Modelle. Wissenschaftler und Entwickler müssen nachvollziehen können, auf welcher Grundlage die KI zu ihren Vorhersagen oder Empfehlungen kommt. Dies stärkt das Vertrauen in die Ergebnisse und erleichtert die Integration von KI-gestützten Erkenntnissen in den Forschungsprozess. Praktisch äußert sich diese Transparenz darin, dass Modelle Verweise auf zugrundeliegende Publikationen oder interne Datenquellen liefern, vergleichbare Molekülstrukturen anzeigen oder die Abfrage einzelner Datenpunkte erlauben.
Ansätze wie Retrieval-Augmented Generation (RAG), bei denen externe relevante Informationen in Echtzeit in die Modellantworten einbezogen werden, helfen dabei, Erklärbarkeit und Glaubwürdigkeit zu erhöhen. Die Rolle von KI-Agenten hat 2025 ebenfalls an Bedeutung gewonnen. Insbesondere generative KI-Assistenzsysteme erleichtern Forschern ihre tägliche Arbeit in vielfacher Hinsicht. Dokumentation, Prototypentwicklung und datengetriebene Informationssuche werden menschengleich unterstützt, was die Effizienz erhöht und kreative Ressourcen freisetzt. Große Sprachmodelle wie GPT werden im Zusammenspiel mit internen Datenbanken dafür eingesetzt, Anfragen innerhalb komplexer Datenlandschaften zu beantworten und somit Daten-Silos aufzubrechen.
Diese technische Innovation erlaubt es Teams, schneller zu erkennen, welche Verbindungen zwischen Molekülen, Studien und Wirkmechanismen bestehen, ohne langwierige Recherchen manuell durchführen zu müssen. Unternehmen wie Certara demonstrieren dies eindrucksvoll, indem sie KI nutzen, um den Design-Make-Test-Analyze (DMTA)-Zyklus zu schließen. KI-basierte Systeme helfen dabei, aus unstrukturierten chemischen Forschungsdaten relevante Erkenntnisse zu extrahieren und visualisieren diese verständlich für Forscher. Dies erhöht nicht nur die Qualität der Entwicklung, sondern beschleunigt zugleich den Innovationsprozess und verringert Fehleinschätzungen. Auch die Pharmaindustrie selbst zeigt zunehmende Pragmatik im Umgang mit KI.
Novartis beispielsweise nutzt mithilfe von RAG-basierten Techniken die enormen Mengen interner Berichte und Forschungsdokumente, welche bislang als unüberschaubarer Wissensschatz galten und kaum systematisch zugänglich waren. Durch Kombination von KI und systematischer Datenintegration werden verborgene Zusammenhänge sichtbar gemacht, die neue Perspektiven für die Wirkstoffentwicklung eröffnen. Trotz aller positiven Fortschritte bleiben Herausforderungen bestehen, die eine schnelle und umfassende KI-Adoption erschweren. Besonderes Augenmerk gilt der Qualität und Verlässlichkeit der KI-Modelle. Die Problematik von „Halluzinationen“, also falsch generierter oder nicht belegbarer Aussagen durch die Modelle, macht die Notwendigkeit einer ständigen Validierung deutlich.
Ebenso sind kognitive Verzerrungen, wie Bestätigungsfehler, nach wie vor Thema. Nutzende Teams müssen sich dieser Limitationen bewusst sein und Verfahren implementieren, die eine adäquate menschliche Kontrolle sicherstellen. Darüber hinaus erfordert der Datenschutz im Zeitalter von KI größte Sorgfalt. Sensible Forschungsdaten dürfen nicht unbeabsichtigt offengelegt oder missbraucht werden. Die Schaffung von klaren Regeln, häufig in Form von Guardrails, und die Einhaltung von Compliance-Anforderungen sind unentbehrlich.
Dies führt auch zu einer Verantwortung der Software- und Plattformanbieter, entsprechende Vorkehrungen und Technologien anzubieten, um den rechtlichen Anforderungen gerecht zu werden. Ein Vergleich mit der Einführung von Cloud-Technologien zeigt interessante Parallelen. Wie die Cloud ist auch KI lange vorbereitet, bevor sie innerhalb eines kurzen Zeitraums explodiert und in nahezu allen Bereichen Anwendung findet. Beide Technologien ersetzen bestehende Systeme nicht vollständig, sondern ergänzen und erweitern die vorhandene Infrastruktur. Im Fall von KI bedeutet dies konkret, dass Forscher durch KI-Tools unterstützt werden – aber die menschliche Expertise und Erfahrung nach wie vor essentiell bleibt.
Die Zukunft der KI in der Wirkstoffforschung sieht vielversprechend aus. Immer stärkere Modelle, verbesserte Datenintegration, und die Etablierung standardisierter Prozesse ermöglichen eine noch engere Verzahnung von KI und wissenschaftlicher Methodik. Zugleich bleibt die Balance zwischen Innovation und verantwortungsvollem Umgang mit Technologie eine Schlüsselaufgabe für Unternehmen und Forscher. Insgesamt lässt sich feststellen, dass im Jahr 2025 die Grundlage geschaffen ist für eine intelligentere, effizientere und transparentere Wirkstoffentwicklung. Die Integration von KI gewinnt an Reife, ist breit akzeptiert und bietet greifbare Vorteile, ohne dabei Risiken zu vernachlässigen.
Für die kommenden Jahre ist zu erwarten, dass dieser Prozess weiter voranschreitet und die Rolle von KI in der Arzneimittelforschung deutlich wachsen wird – zum Nutzen der Wissenschaft, der Industrie und letztlich der Patienten weltweit.