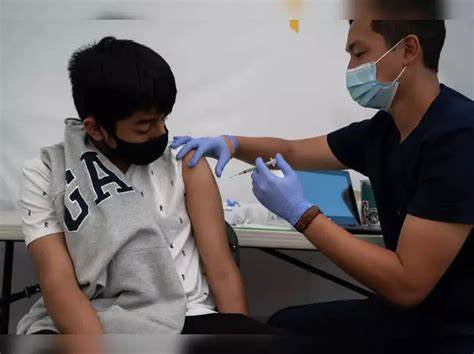
Im Jahr 2025 hat die US-amerikanische Food and Drug Administration (FDA) eine bedeutende Änderung in der Zulassungspolitik für COVID-19-Impfstoffe vorgenommen. Statt wie zuvor eine jährliche Auffrischimpfung für alle Amerikaner ab sechs Monaten zu empfehlen, wird die Impfung nun vor allem für ältere Menschen und Personen mit erhöhtem Risiko beschränkt. Diese neue Regelung sorgt für kontroverse Diskussionen innerhalb der medizinischen Fachwelt, bei Gesundheitsexperten und der allgemeinen Bevölkerung. Die veränderte Impfstrategie zielt darauf ab, den Nachweis von Wirksamkeit und Sicherheit durch umfassendere und längere klinische Studien zu stärken. Die FDA fordert hierzu neue Studien für Produkte, die für gesunde Erwachsene ohne Risikofaktoren zugelassen werden sollen.
Insbesondere sollen Personen zwischen 50 und 64 Jahren in klinische Studien eingeschlossen werden, um die Wirksamkeit der angepassten Impfstoffe detaillierter zu prüfen. Diese Vorgehensweise steht im starken Gegensatz zur bisherigen „One-size-fits-all“-Politik, die eine jährliche COVID-19-Auffrischung für die breite Bevölkerung vorsah – ähnlich der Influenza-Impfung. Bisher konnten aktualisierte Impfstoffe basierend auf ihrem immunologischen Schutz ohne aufwändige Studien zugelassen und breit ausgerollt werden. Experten wie Dr. Vinay Prasad, der kürzlich als leitender FDA-Beamter für Impfstoffe eingestellt wurde, beschreiben den neuen Ansatz als „vernünftigen Kompromiss“.
Er hofft, dass die Impfungen für die besonders gefährdeten Gruppen weitergeführt werden, während gleichzeitig bessere Erkenntnisse für die Frage gewonnen werden, ob gesunde Menschen diese Auffrischungen weiterhin benötigen. Trotz der wissenschaftlichen Argumente wirft die geänderte COVID-19-Impfstoffpolitik jedoch praktische und ethische Fragen auf. Es bleibt unklar, wie Apotheker und medizinisches Personal zukünftig bewerten sollen, ob jemand zu einer Hochrisikogruppe gehört. Kritiker wie der renommierte Impfstoffexperte Dr. Paul Offit warnen, dass diese Einschränkungen die Verfügbarkeit von Impfungen erschweren könnten und möglicherweise zu einem Rückgang der Versicherungsabdeckung führen.
Für Eltern bedeutet die neue Regelung ebenfalls eine Einschränkung der Wahlmöglichkeiten für ihre Kinder. Die American Academy of Pediatrics hat sich besorgt gezeigt, da eine limitierte Impfstoffverfügbarkeit gerade für Kinder aus sozial benachteiligten Familien bedeuten könnte, dass diese weniger Schutz vor COVID-19 genießen. Die Problematik einer potenziell eingeschränkten Erstattung durch Versicherungen könnte zudem weitere Barrieren involvieren. Auch wenn durch COVID-19 im vergangenen Jahr immer noch rund 47.000 Todesfälle in den USA zu verzeichnen waren, darunter Hunderte von Kindern, ist die Gefahrenlage für gesunde Menschen weiteren Altersgruppen umstritten.
Die Behörden und Wissenschaftler diskutieren intensiv darüber, ob jährlich wiederholte Auffrischungen für alle erforderlich sind, oder ob eine Konzentration auf Risikogruppen sinnvoller ist. Die Umorientierung der US-Politik erfolgt unter Leitung von Robert F. Kennedy Jr., dem Gesundheitsminister seit Februar 2025, der im Verlauf seiner Amtszeit mehrere Kritiker der bisherigen Impfstoff-Strategien in führende Positionen eingesetzt hat. Die von ihm geführte FDA verfolgt seitdem eine viel kritischere Haltung gegenüber einer breiten Impfkampagne.
Zuletzt wurde auch der Impfstoff des Herstellers Novavax trotz vollständiger Zulassung nur mit erheblichen Einschränkungen bezüglich der Zielgruppen freigegeben. Diese restriktiven Vorgaben spiegeln sich nun in der generellen Impfstoffpolitik wider und unterstreichen den Fokus auf die Bewertung und Absicherung von Sicherheits- und Wirksamkeitsdaten bei einem enger definierten Kreis von Impfempfängern. Die Hersteller der bislang am meisten eingesetzten mRNA-Vakzine, Pfizer und Moderna, möchten weiterhin mit der FDA kooperieren und ihre Impfstoffe weiterentwickeln. Gleichwohl ist offen, wie sich die politischen und regulatorischen Rahmenbedingungen weiterentwickeln werden, zumal in Europa teilweise andere Empfehlungen gelten, die beispielsweise Jahresauffrischungen weniger pauschal, sondern stärker differenziert nach Alter und individuell erhöhtem Risiko aussprechen. Im laufenden Prozess ist auch der Einfluss des bevorstehenden CDC-Beratungsgremiums relevant, welches im Juni 2025 Empfehlungen zu Impfungen und Auffrischungen für unterschiedliche Alters- und Risikogruppen abgeben soll.
Kritiker wie Dr. Offit sehen mit Sorge, dass die FDA bereits eigene Richtlinien vorlegt und damit den Beratungsprozess des CDC uminterpretiert. Für die Bevölkerung bedeutet die neue Politik eine Umstellung und weitere Herausforderungen. Während ältere Menschen und Risikogruppen weiterhin Zugang zu Schutzimpfungen haben, werden gesunde und jüngere Erwachsene sowie viele Familien durch die Restriktionen bei der COVID-19-Vakzinierung vor schwer absehbare Barrieren gestellt. Diese Entwicklungen finden zudem in einem Umfeld statt, in dem das Vertrauen in Impfprogramme und Gesundheitsbehörden herausgefordert wird.