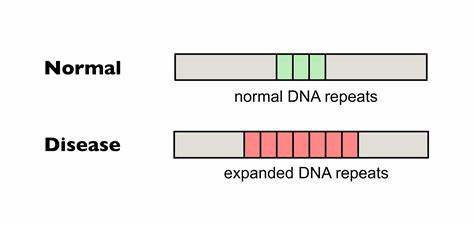
Huntington ist eine verheerende neurodegenerative Erkrankung, die genetisch bedingt durch die Expansion von sogenannten trinukleotiden Wiederholungen im HTT-Gen ausgelöst wird. Diese CAG-Wiederholungen kodieren für eine Polyglutamin-Kette im Huntingtin-Protein, deren verlängerte Form toxisch für Neuronen ist. Der pathogene Mechanismus der Krankheit hängt nicht nur von der Länge der Wiederholung bei der Geburt ab, sondern auch von der somatischen Instabilität dieser Wiederholungen, das heißt ihrer weiteren Expansion in Geweben wie dem Gehirn im Laufe des Lebens. Diese somatischen Erweiterungen tragen maßgeblich zum Fortschreiten der Krankheit bei und beeinflussen sowohl das Alter des Krankheitsbeginns als auch die Schwere der Symptome. In den letzten Jahren hat die Wissenschaft enorme Fortschritte im Bereich der Genom-Editierung gemacht, insbesondere mit der Entwicklung von sogenannten Base Editoren, die nukleotidgenaue Veränderung im Erbgut ermöglichen, ohne die DNA-Stränge komplett zu schneiden.
Forscher haben nun diese Technologie eingesetzt, um gezielt die trinukleotiden Wiederholungen im HTT-Gen zu bearbeiten, indem sie subtil die Folge der Basen in den CAG-Trinukleotiden verändern, ohne die kodierte Aminosäuresequenz des Proteins zu verändern. Diese sogenannten „Interruptions“ in der Wiederholung können die Instabilität der Sequenz vermindern und somit die somatische Expansion reduzieren. Die Strategie basiert auf der Erkenntnis, dass bestimmte natürliche Varianten in humanen Populationen, in denen einzelne CAG-Abschnitte durch CAA-Codons unterbrochen werden, mit milderen Krankheitsverläufen und einer Verzögerung des Symptombeginns einhergehen. Deshalb haben Wissenschaftler versucht, mithilfe von Cytosin-Baseneditoren gezielt einzelne CAG-Tripletts in CAA umzuwandeln, was aufgrund der identischen Polyglutamin-Codierung der beiden Triplets (beide kodieren für Glutamin) keine Veränderung im Huntingtin-Protein verursacht, jedoch die DNA-Sequenz herausfordernder für somatische Expansionen macht. Experimentelle Studien in Patientenzellen zeigten beachtliche Erfolge: Durch das Einbringen dieser Interruptions konnte die Häufigkeit der längeren, pathogenen Wiederholungstrakte im HTT-Gen deutlich reduziert werden.
Dabei zeigte sich, dass die durch Base Editing induzierten Veränderungen die somatische Expansion nicht nur stoppen, sondern in bestimmten Zellkulturen sogar eine Kontraktion der Wiederholungen bewirken konnten. Diese Ergebnisse sind besonders vielversprechend, da sie eine direkte Modifikation des genetischen Ursprungs der Krankheit darstellen. Auch in Tiermodellen, wie etwa HD-Mauslinien, die humane HTT-Gene mit pathogenen CAG-Expansionen tragen, führte die Abgabe von Base Editing-Strategien mittels AAV9-Viralen Vektoren zu einer signifikanten Reduktion der somatischen Instabilität in Gehirnregionen, die typischerweise von der Krankheit betroffen sind, wie dem Cortex und Striatum. Die Effizienz der Editierung stieg mit der Zeit und manifestierte sich langfristig in einer signifikanten Verminderung der Expansionen der CAG-Wiederholungen. Das ist ein bedeutsamer Fortschritt, denn es zeigt, dass eine Einmalbehandlung in der frühen postnatalen Phase die neurodegenerativen Prozesse der Huntington-Erkrankung zumindest auf molekularer Ebene bremsen kann.
Ein wichtiger Aspekt bei dieser Technologie ist die hohe Spezifität und der Umgang mit möglichen Off-Target-Effekten. In ausgiebigen genomweiten Analysen zeigten die Forscher, dass die meisten Baseneditor-bedingten Veränderungen an Wiederholungssequenzen entweder keine proteinkodierenden Veränderungen nach sich zogen oder Synonyme Substitutionen waren, die die Proteinstruktur nicht beeinflussen. Nur eine sehr geringe Anzahl von Nonsynonymen Mutationen trat auf, und darunter waren wenige potenziell funktionell relevante Veränderungen, weshalb weitere Sicherheitsuntersuchungen erforderlich sind. Dennoch deuten die bisherigen Daten auf ein günstiges Sicherheitsprofil hin. Die Wichtigkeit der somatischen Wiederholungsexpansion bei der Pathogenese von Huntington wird durch diese Studien eindrucksvoll unterstrichen.
Sie bestätigen, dass die reine Verlängerung der CAG-Wiederholungsstrecke nicht das alleinige Problem ist, sondern vor allem deren progressive Expansion in zentralnervösen Zellen die Neurodegeneration vorantreibt. Somit steht die somatische Instabilität auch als vielversprechendes therapeutisches Ziel im Fokus. Neben Huntington wird eine ähnliche Base Editing-Technologie bei anderen TNR-Erkrankungen wie Friedreich-Ataxie untersucht, wobei hier die Adenin-Baseneditoren verwendet werden, um GAA-Wiederholungen zu unterbrechen und ebenfalls die somatische Expansion zu verringern. Die Übertragung dieses Konzepts auf unterschiedliche genetische Krankheiten eröffnet neue Horizonte für die Behandlung bisher unheilbarer neurodegenerativer Erkrankungen. Die Herausforderung bleibt, die Base Editing-Technologie sicher, effektiv und breitflächig im Menschen anzuwenden.
Probleme wie dauerhafte Expression von Base-Editoren nach viraler Abgabe, mögliche Immunreaktionen, effiziente Zielgewebeansteuerung und Verhinderung unerwünschter genetischer Veränderungen erfordern weitere Forschung. Derzeit werden verschiedene Ansätze verfolgt, um die Liefermethoden zu verfeinern, etwa durch Virus-ähnliche Partikelsysteme, lipidbasierte Nanopartikel oder kontrollierte, kurzzeitige Expression in Zielzellen. Insgesamt markieren die jüngsten Fortschritte beim gezielten Editieren von trinukleotiden Wiederholungen in Huntington-Patientenzellen einen Meilenstein in der Gentherapie. Die Fähigkeit, somatische CAG-Expansionen zu unterbrechen und sogar zu reduzieren, bietet neues therapeutisches Potenzial, um das Fortschreiten dieser schweren Erkrankung zu verlangsamen oder womöglich zu stoppen. Diese Entwicklungen ermutigen zu weiterführenden präklinischen und klinischen Studien, die letztlich die Lebensqualität von Betroffenen verbessern könnten.
Der Fokus auf präzise Modifikation der DNA-Sequenz an kritischen Wiederholungsstellen ohne Beeinträchtigung der ursprünglichen Proteinstruktur stellt einen innovativen Paradigmenwechsel in der Behandlung von Huntington und verwandten TNR-Erkrankungen dar. Sprachrohr für diese Fortschritte ist ein multidisziplinäres Feld aus Molekularbiologie, Genetik, Neurologie und Bioengineering, das mit vereinten Kräften wegweisende Therapien für zuvor unheilbare Krankheiten erarbeitet. Zukünftige Forschung wird sich darauf konzentrieren, wie diese molekularen Eingriffe in komplexe neuronale Netzwerke und die Pathophysiologie der Krankheit eingreifen, welche Langzeitwirkungen zu erwarten sind und wie man individuelle genetische Variationen in Patientengruppen berücksichtigt. Auch ethische und regulatorische Aspekte der Genom-Editierung spielen eine bedeutende Rolle für die Etablierung dieser Therapieformen. Somit stehen wir an der Schwelle zu einer neuen Ära in der Behandlung von Huntington, die direkt an der Wurzel des genetischen Defekts ansetzt.
Mit weiteren technologischen Optimierungen und rigorosen Sicherheitsprüfungen wird das gezielte Editieren von Trinukleotid-Wiederholungen zu einem unverzichtbaren Werkzeug in der personalisierten Medizin gegen neurodegenerative Erbkrankheiten avancieren.