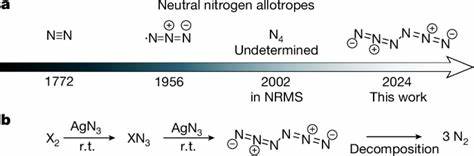
Stickstoff, das am häufigsten vorkommende Element in unserer Atmosphäre, ist als molekulares N2 aufgrund seiner starken Dreifachbindung äußerst stabil und inert. Trotz dieser Stabilität gilt die Forschung an höheren neutralen Stickstoff-Allotropen seit Jahrzehnten als eine der größten Herausforderungen der modernen Chemie. Polynitrogene, auch als Stickstoff-Allotrope bezeichnet, versprechen als hochenergetische Materialien enorme Energiemengen freizusetzen, ohne dabei schädliche Rückstände zu hinterlassen – allein harmloses N2 als Zerfallsprodukt. Bislang beschränkte sich die isolierbare neutrale molekulare Form des Stickstoffs auf das Diatom N2. Alles darüber hinaus war bislang vorrangig theoretischer Natur oder nur als kurzlebiges Zwischenprodukt nachweisbar.
Die kürzlich publizierte Studie von Qian, Mardyukov und Schreiner in Nature stellt einen bemerkenswerten Durchbruch dar. Es wurde erstmals eine neutrale, molekulare Stickstoff-Allotrop-Form namens Hexanitrogen (C2h-N6) erfolgreich synthetisiert und bei Raumtemperatur nachgewiesen. Die Herstellung erfolgte durch die Reaktion von Chlor- beziehungsweise Brom mit Silberazid (AgN3) im Gasphasenverfahren und das anschließende Einfangen der Reaktionsprodukte in argonbasierten Matrixen bei 10 Kelvin. Zusätzlich konnte reines N6 als dünner Film bei flüssigem Stickstoff (77 Kelvin) auf einer Matrixoberfläche stabilisiert werden, was die überraschende Standfestigkeit dieser außergewöhnlichen Stickstoffform betont. Die Bedeutung dieser Entdeckung liegt nicht nur in der erstmaligen experimentellen Realisierung eines neutralen Stickstoffmoleküls jenseits des stabilen N2, sondern auch in ihrem Potenzial für Innovationen im Bereich der High-Energy-Density Materials (HEDM), das heißt Materialien mit hoher Energiedichte.
Polynitrogene bieten aufgrund ihrer hohen Energiegehalte, die jene von Wasserstoff, Ammoniak oder Hydrazin übertreffen, eine potenziell saubere Alternative für Energiespeicherung und -freisetzung. Im Vergleich zu herkömmlichen Explosivstoffen wie TNT oder HMX übertrifft die theoretisch berechnete Energieausbeute des N6 die von TNT sogar um das Zweieinhalbfache, was es zu einem sehr interessanten Kandidaten für zukünftige Anwendungen macht. Die experimentelle Bestätigung des N6 wurde durch eine Kombination aus Infrarot- und UV-Vis-Spektroskopie, 15N-Isotopenmarkierung und hochpräzisen quantenchemischen Berechnungen ermöglicht. Diese Methoden zeigten charakteristische Signale, die mit dem theoretisch vorhergesagten Vibrationsspektrum übereinstimmen und bewiesen, dass es sich bei den neuen Spektrallinien tatsächlich um das Hexanitrogen handelt. Einer der entscheidenden Hinweise war die Identifikation eines intensiven Infrarotbandes bei 2076,6 cm−1, das zum asymmetrischen Streckschwingung von Azid-Radikalen vergleichbar ist.
Computergestützte Untersuchungen zum Energieprofil und zur Molekülstruktur bestätigten, dass das C2h-konfigurierte N6 ein lokales Minimum im energetischen Sinne bildet und somit kinetisch stabil genug ist, um bei Raumtemperatur existieren zu können. Während viele mögliche strukturale Isomere von Polynitrogen vorausberechnet wurden, weist dieses Modell eine signifikant höhere Barriere gegen spontane Zersetzung auf als zuvor betrachtete Verbindungen, was die praktische Synthese und Stabilität erst ermöglicht. Die zentrale N–N-Bindung in diesem Molekül ist weniger anfällig für spontane Dissoziation, da der Zerfallsweg in drei Stickstoffmoleküle mit einer Aktivierungsenergie von etwa 14,8 kcal/mol verbunden ist. Dies verleiht dem Molekül eine ausreichend lange Halbwertszeit, sodass es experimentell nachweisbar ist. Besonders bemerkenswert sind die quantenmechanischen Berechnungen zum Zerfall über den sogenannten quantenmechanischen Tunneleffekt (Quantum Mechanical Tunneling, QMT).
Während viele potentielle Stickstoff-Allotrope durch QMT eine extrem kurze Lebensdauer besitzen, weist das N6 eine deutlich längere Abschätzung der Lebensdauer auf – im Bereich von Jahren oder zumindest Millisekunden bei Raumtemperatur, was die Beobachtung in Kryomatrizen erklärt. Diese Stabilität ist für die praktische Handhabung ein wichtiger Faktor. Den Syntheseweg prägt die Reaktion von AgN3 mit Chlor- oder Brommolekülen im reduzierten Druck, bei der gasförmige Halogene über das Silberazid geleitet werden. Silberazid ist bekannt als ein ausgezeichneter Ausgangsstoff für die Herstellung von Aziden und Halogenahydroxyderivaten und reagiert entsprechend in der Gasphase zu dem Zielmolekül. Die erzeugten Moleküle werden anschließend in einer extrem kalten Argonmatrix isoliert, um die Reaktionsergebnisse direkt zu analysieren.
Die isolierten N6-Moleküle zeigen weitere Beweise ihrer Existenz durch isotopenmarkierte Experimente mit 15N, wobei sich die Spektralbänder verschieben, was die Vermutung über ihre Struktur untermauert. Darüber hinaus konnte reines N6 ohne Wirtsmatrix bei niedrigen Temperaturen (77 K) gefilmt und stabil gehalten werden. Die Ähnlichkeit der photochemischen Reaktionsmuster mit denen in der Argonmatrix weist darauf hin, dass N6 ausreichend robust ist, um in der reinen Form erhalten zu bleiben, was die Tür für mögliche Anwendungen öffnet. Ein wichtiger Aspekt ist die Molekülstruktur des N6, die sich durch zwei azideähnliche N3-Einheiten auszeichnet, die über eine zentrale Bindung verknüpft sind mit C2h-Symmetrie. Die bindenden Eigenschaften zeigen eine Kombination aus Doppel- und Einfachbindungen zwischen den Stickstoffatomen, was durch theoretische Bond-Order-Analysen und Ladungsverteilungen bestätigt wird.
Diese ist substantiell verschieden von bekannten Stickstoffmolekülen wie dem Azid-Radikal oder dem Diazenmolekül, jedoch mit einer vergleichbaren elektronischen Verteilung in den Bindungen. Die Möglichkeit, solche Polynitrogene in neutraler Form zu synthetisieren, indem ausschließlich Stickstoffatome beteiligt sind, markiert einen historischen Wendepunkt in der Chemie des Stickstoffs. Die bisherigen Studien konzentrierten sich meist auf polynitrogene Ionen, wie das pentanitrogene Anion cyclo-N5–, welches teils stabilisiert in Salzen isoliert werden konnte. Die Synthese neutraler, ungeladener polynitrogener Moleküle war jedoch stets eine große Herausforderung aufgrund der inhärenten Instabilität dieser Spezies. Zusätzlich zu ihrem wissenschaftlichen Wert bietet das neutrale Hexanitrogen ein großes Potenzial für Anwendungen in der Energiespeicherung, sprengstoffähnlichen Systemen und möglicherweise als Ausgangsmaterial für die Entwicklung nachhaltiger Kraftstoffe.
Die Freisetzung von Energie bei der Zersetzung in N2-Moleküle erfolgt umweltfreundlich, da lediglich atmosphärischer Stickstoff zurückbleibt, der keine Schadstoffe oder Treibhausgase verursacht. Die Entdeckung fordert somit etablierte Vorstellungen in der Chemie heraus und öffnet den Weg für weitere Forschungen, um die Synthese anderer ursprünglich als hypothetisch geltender Moleküle zu ermöglichen. Ferner liefern die angewandten Methoden der Kombination von experimenteller Matrixisolation, photonischer Zersetzung und hochgenauer Rechenchemie ein starkes Modellsystem für zukünftige Studien im Bereich der hochenergetischen molekularen Materialien. Abschließend lässt sich sagen, dass die Herstellung von neutralem Hexanitrogen C2h-N6 einen großen Fortschritt in der Wissenschaft darstellt. Es wurde bewiesen, dass neutral-polynitrogene Moleküle existieren und stabilisiert werden können, was zu potenziell revolutionären Anwendungen in der Materialwissenschaft und Energiebranche führen kann.
Die Ergebnisse ermutigen zur intensiven weiteren Erforschung dieses Bereiches mit dem Ziel, die Grenzen der Molekülchemie neu zu definieren und innovative Materialien für die Zukunft zu entwickeln.



![RTX Pro 6000: Skip M3 Ultra and RTX 5090 for LLMs with the New 96GB King [video]](/images/6061CDB3-B411-4CAB-A221-D3578C836B03)