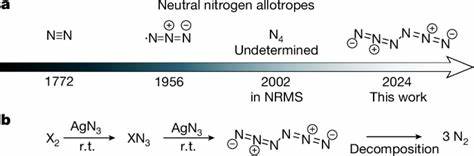
Stickstoff ist eines der häufigsten Elemente auf der Erde und bildet mit zweiatomigen Molekülen (N2) die Hauptkomponente unserer Erdatmosphäre. Seit langem gilt molekularer Stickstoff als besonders stabil und inert, was ihm eine zentrale Rolle in biologischen und industriellen Prozessen zuschreibt. Allerdings beschränkte sich die Wissenschaft bis vor Kurzem auf die Existenz des stabilen zweiatomigen Stickstoffs als einzigem neutralen Stickstoffallotrop. Die Synthese von neutralen, komplexeren Stickstoffmolekülen jenseits von N2 galt als außerordentlich schwierig, da diese Verbindungen meist hochreaktiv und instabil sind. Mit der erfolgreichen Herstellung des neutralen Hexanitrogens C2h-N6 hat sich dieses Paradigma nun grundlegend gewandelt.
Die Entdeckung ist ein Meilenstein, der nicht nur die Grenzen der chemischen Synthese verschiebt, sondern auch neue Wege in der Entwicklung von Hochenergiematerialien ebnet. Das Hexanitrogenmolekül C2h-N6 besteht aus sechs Stickstoffatomen in einer spezifischen Anordnung und zeigt eine außergewöhnliche Stabilität für eine solche polynitrogene Struktur. Die Synthese gelingt durch eine innovative gasphasige Reaktion zwischen Halogenen wie Chlor oder Brom und Silberazid unter kontrollierten Bedingungen bei Raumtemperatur. Anschließend wird das entstehende Produkt in Argonmatrizes bei extrem niedrigen Temperaturen (10 Kelvin) gefangen, wodurch seine Stabilität weiter erhöht und eine detaillierte spektroskopische Untersuchung ermöglicht wird. Die Möglichkeit, das gereinigte N6 auch als dünne Filmform bei Flüssigstickstofftemperatur (77 Kelvin) herzustellen, unterstreicht die praktische Relevanz dieser Substanz.
Die Bedeutung der Entdeckung leitet sich sowohl aus den theoretischen als auch aus den experimentellen Aspekten ab. Theoretische Berechnungen, die auf hochpräzisen Methoden wie dem CCSD(T) Verfahren basieren, bestätigen die Stabilität des N6-Moleküls als lokales Minimum auf der potentiellen Energieoberfläche. Dies bedeutet, dass das Molekül kinetisch stabil genug ist, um nicht sofort zu zerfallen, was bei früheren Versuchen an größeren Stickstoffclustern zumeist nicht der Fall war. Die Computermodelle zeigen, dass die Bindungen innerhalb des Moleküls charakteristische Längen und Stärken besitzen, die denen einzelner Stickstoffbindungen in Verbindungen wie Diazene oder Hydrazin ähneln. Besonders interessant ist die Betrachtung der Elektronendichteverteilung mittels Laplacian- und Elektronenlokalisationsfunktionsanalysen, die identifizierbare „Schwachstellen“ für die Bindungsspaltung aufzeigen, jedoch dennoch relativ hohe Aktivierungsbarrieren für den Zerfall in einfachere Stickstoffmoleküle vorhersagen.
Ein wesentlicher Faktor für die Stabilität von Hexanitrogen ist die energetische Barriere, die für die Zersetzung in drei Moleküle des stabilen N2 überwunden werden muss. Mit einem berechneten Aktivierungsenthalpiewert von etwa 14,8 kcal/mol ist diese Barriere vergleichsweise hoch, was auf eine ausreichende Lebensdauer des N6-Moleküls auch bei Raumtemperatur hinweist. Darüber hinaus sind quantenmechanische Tunnelungseffekte, die typischerweise bei kleineren Stickstoffclustern zu einer schnellen Zersetzung führen können, für das C2h-N6 weniger relevant. Modelle schätzen sogar eine Halbwertszeit im Millisekundenbereich bei Raumtemperatur und in der Größenordnung von Jahrzehnten bei tiefen Temperaturen, was experimentell durch das erfolgreiche Einfangen in Matrix und Darstellung als Film bestätigt wird. Zur experimentellen Identifikation des Hexanitrogens dienen insbesondere spektroskopische Methoden wie Infrarotspektroskopie sowie UV-Vis-Spektrometrie.
Dabei konnten charakteristische Vibrationsbanden bei Wellenzahlen von beispielsweise 2076,6 cm−1 identifiziert werden, die sich durch Isotopenmarkierung mit Stickstoff-15 weiter verifizieren ließen. Die Verschiebung und Aufspaltung der Banden bei den verschiedenen markierten Isotopologen stimmt exakt mit theoretischen Vorhersagen überein, was die Zuordnung der Signale zum intrinsischen N6-Molekül festigt. Die Möglichkeit, das Molekül per Lichtbestrahlung bei 436 nm gezielt zu zerlegen und dabei das Verschwinden der charakteristischen Banden zu beobachten, liefert zusätzliche überzeugende Belege für die Existenz und Struktur des Hexanitrogens. Die Konsequenzen dieser Entdeckung sind weitreichend. Die Tatsache, dass hexanitrogenhaltige Verbindungen eine enthalpische Zersetzung aufweisen, die mehr als doppelt so hoch ist wie bei klassischen Sprengstoffen wie TNT oder HMX, eröffnet Potenziale in der Entwicklung von Hochenergiematerialien.
Da die Zersetzung reines, harmloses Stickstoffgas freisetzt, bestehen zudem ökologische Vorteile gegenüber üblichen Energieträgern und Sprengstoffen, die toxische oder treibhauswirksame Nebenprodukte erzeugen. Die Herausforderung bleibt jedoch die praktische Handhabung, da die Reaktivität trotz der relativen Stabilität weiterhin hoch bleibt und Sicherheitsvorkehrungen bei der Herstellung und Lagerung von Silberazid und Halogenaziden zwingend notwendig sind. Neben der materiellen Anwendung bietet das Hexanitrogen fundamentale Erkenntnisse über die Chemie der Polymerelemente. Während der Kohlenstoff als Allotrop vielfältige Formen wie Graphit, Diamant, Fullerene und zahlreiche weitere komplexe Strukturen bildet, ist das Element Stickstoff durch seine hohe Elektronegativität und geringe Neigung zur Mehrfachbindung in größeren Molekülen wesentlich restriktiver. Die Synthese eines stabilen neutralen N6 zeigt, dass auch bei Stickstoff unter geeigneten Bedingungen komplexere Allotrope möglich sind und erweitert somit das Verständnis chemischer Bindungen und elektronischer Strukturen.
Diese Erkenntnisse können zu weiteren Untersuchungen und eventuell zur Entdeckung anderer stickstoffbasierter polymolekularer Strukturen führen, die bisher nur theoretisch betrachtet wurden. Ein weiterer wissenschaftlicher Aspekt betrifft die besondere Symmetrie des C2h-N6. Die Molekülstruktur unterscheidet sich von zuvor vorgeschlagenen zyklischen Formen wie der hexazinartigen Ringform (cyc-N6), die theoretisch zwar aromatisch konzipiert wurde, jedoch durch sehr niedrige Aktivierungsbarrieren unmittelbar in N2 zerfällt. Die acyclische N6-Form mit C2h-Symmetrie weist dagegen eine signifikant höhere kinetische Stabilität auf und widerlegt die früher verbreitete Annahme, dass neutrale Polynitrogene jenseits von N2 nicht zu isolieren sind. Die experimentelle Realisierung eröffnete sich durch die geschickte Kombination von Silberazid mit Halogenmolekülen in der Gasphase.
Silberazid ist ein seit langem bekanntes explosives Material, das in dieser Reaktion als Quelle für das Azid-Radikal dient. Die kontrollierte Reaktion mit Chlor oder Brom ermöglicht eine gezielte Verknüpfung von Azidfragmenten zu längeren Stickstoffketten, deren Produkt in der ultrakalten Matrix eingefangen wird. Die dabei verwendeten Techniken zur Matrixisolierung sind unerlässlich, um die fragile Verbindung aufzustabilisieren und genaue spektroskopische Daten zu gewinnen. Die Fortschritte in der Rechenchemie haben wesentlich zur Identifikation und zum Verständnis von Hexanitrogen beigetragen. Moderne Dichtefunktionaltheorien (DFT) und hochgenaue Korrelationsmethoden ermöglichen nicht nur die Vorhersage von Molekülstrukturen, Vibrationsfrequenzen und elektronischen Übergängen, sondern auch realistische Abschätzungen von Reaktionsbarrieren und Zerfallskinetiken.
Dies war entscheidend, um Vermutungen über die Instabilität der Stickstoffverbindungen zu überprüfen und gezielt experimentelle Bedingungen zu schaffen, unter denen N6 erzeugt und dauerhaft nachgewiesen werden konnte. Die Veröffentlichung dieser Erkenntnisse in einem renommierten Journal wie Nature verdeutlicht den wissenschaftlichen Stellenwert und weckt Erwartungen an zukünftige Forschungsschritte. Mögliche Fragestellungen umfassen die Stabilisierung noch größerer neutraler Stickstoffallotrope, die Untersuchung von Festkörperformen basierend auf N6 und deren energetisches Potential, sowie die Erforschung von katalytischen oder photochemischen Reaktionen, die unter Einsatz von Polynitrogenen neuartige Synthesen erlauben könnten. Zusammenfassend stellt die Herstellung und Spezifizierung von Hexanitrogen C2h-N6 eine Revolution im Bereich der polymolekularen Stickstoffchemie dar. Neben der Erforschung grundlegender chemischer Prinzipien eröffnet sie zugleich Perspektiven auf innovative Energiespeichermaterialien mit einer enorm hohen Energiedichte bei gleichzeitiger Umweltverträglichkeit.
Die Herausforderung bleibt, diese Substanz sicher und wirtschaftlich nutzbar zu machen. Dennoch hat die Entdeckung die Basis für eine neue Ära in der Materialchemie gelegt, in der Stickstoff nicht mehr nur als inert betrachtet wird, sondern als Baustein hochenergetischer und funktionaler Moleküle mit vielfältigen Anwendungsmöglichkeiten.





![Canada's Arctic Sovereignty: Resilience and Change in the Liberal State [pdf] (2022)](/images/0D790299-5E74-4D53-8E2C-CE53D0773291)

