Die steigende Zahl an Krebserkrankungen weltweit stellt die medizinische Forschung vor große Herausforderungen. Trotz zahlreicher Fortschritte in der Immuntherapie und zielgerichteten Therapien bleiben viele Krebsarten schwer zu behandeln, insbesondere solche mit aggressivem Wachstum und hoher Resistenzen. Eine neue vielversprechende Therapieform setzt hier an: die gezielte Modifikation von Adipozyten, den Fettzellen des Körpers, die durch Implantation in Tumorumgebungen das Tumorwachstum hemmen können. Diese innovative Methode trägt die Bezeichnung adipose manipulation transplantation (AMT) und basiert darauf, dass die modifizierten Fettzellen aktiv mit Krebszellen um Nährstoffe konkurrieren, was das Krebswachstum effektiv reduziert. Tumoren sind hochgradig metabolisch aktiv und passen ihren Stoffwechsel an die oft nährstoffarmen, hypoxischen Bedingungen im Tumormikromilieu an.
Sie bevorzugen die sogenannte aerobe Glykolyse, auch Warburg-Effekt genannt, bei der sie vermehrt Glukose aufnehmen und zu Lactat metabolisieren, selbst wenn ausreichend Sauerstoff vorhanden ist. Zusätzlich verstärken Tumorzellen unter Sauerstoffmangel die Nutzung von Fettsäuren, da diese als Energiesubstrat gegenüber Glukose einen zweifach höheren Energiegehalt besitzen. Zahlreiche therapeutische Ansätze versuchen daher, die Glukose- und Fettsäureverwertung von Krebszellen gezielt zu beeinflussen und so deren Überleben zu erschweren. AMT verfolgt nun einen völlig anderen Ansatz: Anstatt die Tumorzellen direkt zu hemmen, werden körpereigene Fettzellen so modifiziert, dass sie selbst ihre Glukose- und Fettsäureaufnahme stark erhöhen und den Krebszellen damit „die Nahrung wegnehmen“. Durch genetische Aktivierung von Schlüsselmolekülen wie dem uncoupling protein 1 (UCP1), das normalerweise in braunem Fettgewebe vorkommt und Energie als Wärme dissipiert, werden weiße Adipozyten in einen braun-ähnlichen Zustand versetzt.
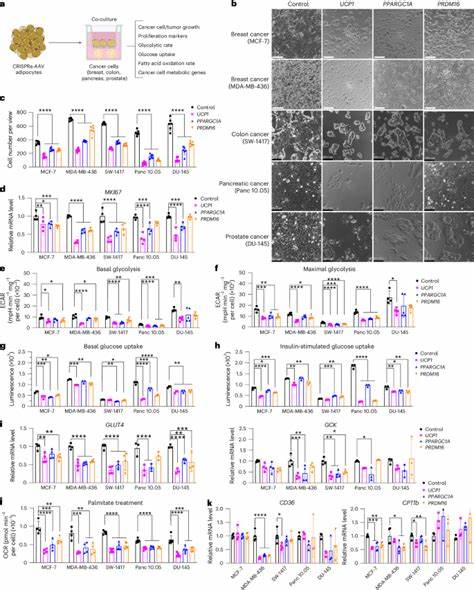
Diese sogenannten beige Adipozyten sind metabolisch besonders aktiv und nehmen erheblich mehr Nährstoffe auf als normale Fettzellen. Das Verfahren beruht auf der CRISPRa-Technologie (CRISPR-Activation), mit deren Hilfe bestimmte Gene in den Adipozyten gezielt aktiviert werden, ohne deren Genom zu verändern. Mit Hilfe eines harmlosen Adeno-assoziierten Virus (AAV) werden die Genaktivatoren zusammen mit Guide-RNAs verabreicht, die die Expression von UCP1 oder anderen Genen wie PPARGC1A oder PRDM16 erhöhen. Diese Modulation löst eine Vermehrung der Sauerstoffaufnahme, der Glukose- und Fettstoffwechselkapazität sowie der Energieverbrauch in den Adipozyten aus. Experimentelle Studien an verschiedenen Krebszelllinien wie Brust-, Kolon-, Pankreas- und Prostatakrebs haben gezeigt, dass kultivierte, genetisch aktivierte Adipozyten das Zellwachstum dieser Tumoren erheblich unterdrücken.
Dabei wird die Proliferation der Krebszellen signifikant reduziert, was durch niedrigere Expression des Zellteilungsmarkers Ki67 dokumentiert wird. Neben der Verminderung der Zellzahl konnte auch ein Rückgang der Glykolyse und Fettsäureoxidation in Tumorzellen beobachtet werden – ein Hinweis darauf, dass diese Energiequellen in der Tumormikroumgebung knapp werden. Im Tiermodell wurden diese Ergebnisse bestätigt, indem CRISPRa-modifizierte menschliche Adipozyten-Organoide zusammen mit Tumorzellen in immunsupprimierte Mäuse transplantiert wurden. Die Gruppe mit den modifizierten Fettzellen zeigte wesentlich kleinere Tumoren, was mit einem signifikanten Rückgang von Hypoxie und Angiogenese im Tumorgewebe einherging. Besonders bemerkenswert war, dass die Implantation nicht nur direkt an der Tumorstelle, sondern auch distal eine tumorhemmende Wirkung erzielte, was die vielversprechende klinische Anwendbarkeit unterstreicht.
Eine weitere Key-Funktion, die diesen Therapieansatz unterstützt, ist die systemische Stoffwechselveränderung. Die modifizierten Adipozyten führen zu einem gesteigerten Gesamtenergieverbrauch, was sich in verbesserter Glukosetoleranz und erhöhter Insulinsensitivität bei behandelten Mäusen zeigt. Gleichzeitig wurden niedrigere Insulinspiegel im Blut festgestellt, was für eine verminderte Wachstumsförderung von Krebszellen günstig ist, da Insulin als Wachstumsfaktor wirkt. Die Vielseitigkeit des Ansatzes zeigt sich auch darin, dass nicht nur Glukose- und Fettstoffwechsel gezielt genutzt werden. So konnte man durch die Aktivierung eines anderen Stoffwechselenzyms, UPP1 (Uridin Phosphorylase 1), die Verwertung von Uridin, einem für bestimmte Pankreaskrebsarten wichtigen Nährstoff, steigern und die Tumorprogression modulieren.
Diese maßgeschneiderte Anpassbarkeit ermöglicht die individuelle Ausrichtung der Therapie auf die unterschiedlichen metabolischen Bedürfnisse und Anpassungen von Tumoren. Neben der Verwendung gentechnisch modifizierter Zelllinien wurde das Potenzial von AMT auch mit Adipozyten aus Patientinnen-gewebebrüchen demonstriert. Diese ex vivo isolierten und über AAV-CRISPRa modifizierten Fettzellen konnten im Co-Kultur-System das Wachstum von patienteneigenen Brustkrebs-Organoiden unterdrücken. Besonders beeindruckend ist die Hemmung präkanzeröser Veränderungen in Brustgewebs-Organoiden von Patientinnen mit erblichen BRCA1/2-Risikomutationen, was präventive Anwendungsperspektiven eröffnet. Um die klinische Umsetzung zu unterstützen, wurde ein induzierbares System mit Tet-On-Mechanismus entwickelt, das eine gezielte und zeitlich steuerbare Aktivierung der therapeutischen Gene mittels Tetrazyklin ermöglicht.
Ebenso wurde die Integration in eine Polymer-Mikrowellschale erforscht, die die kontrollierte Implantation und bei Bedarf Entfernung der modifizierten Fettzellen erlaubt – wichtige Voraussetzungen für eine sichere und anpassbare medizinische Anwendung. Die AMT-Methode zeigt nicht nur innovative Mechanismen, sondern nutzt auch etablierte klinische Techniken. Die Gewinnung von Adipozyten per Liposuktion und deren Transplantation sind routinemäßige Verfahren in der plastischen Chirurgie. Die Kombination mit molekularbiologischer Modifikation zur Stoffwechselmanipulation erschließt ein neues Feld der zellbasierten Krebstherapie. Während konventionelle Therapien oftmals direkt auf Krebszellen abzielen, eröffnet AMT einen vielversprechenden Weg, den Tumor indirekt zu schwächen, indem ihm wichtige Energiequellen vorenthalten werden.
Das macht die Tumorzellen metabolisch vulnerabler und könnte potenziell Resistenzen gegenüber anderen Therapieformen vermindern. Zudem zeigt AMT Vorteile hinsichtlich des Immunstatus: Adipozyten rufen bei Transplantationen keine starke Immunreaktion hervor, was die Entwicklung allogener Zelltherapien erleichtert. Dies hebt diesen Ansatz beispielsweise von CAR-T-Zelltherapien ab, die komplexe Immunmodulation erfordern. Ein wichtiger Aspekt für die Langzeittherapie ist die Kontrolle über die genetische Modifikation und das Überleben der implantierten Zellen. Die Verwendung von induzierbaren Systemen sowie dosierbaren Implantationsplattformen schafft die Möglichkeit, therapeutische Eingriffe flexibel an die Fortschritte oder Rückmeldungen des Patienten anzupassen, Nebenwirkungen zu minimieren und eine Überdosierung zu vermeiden.
Die potenziellen Risiken, die sich zum Beispiel aus einer Überaktivierung des braunen Fettgewebes ergeben könnten, wie z. B. die Entstehung von Kachexie (krankhaftem Gewebeschwund), müssen weiterhin sorgfältig untersucht werden. Die bisher durchgeführten Tierstudien zeigen jedoch keine signifikanten Gewichtsverluste, was Hoffnung auf eine sichere Anwendung gibt. Die Zukunft der AMT-Technologie liegt in der Kombination mit weiteren personalisierten Ansätzen, bei denen Bioinformatik, individuelle Tumorprofilierung und gezielte Genmodifikationen ineinandergreifen, um auf den individuellen Stoffwechsel des Tumors zugeschnittene Zelltherapien zu entwickeln.
Dies könnte die Effektivität deutlich steigern und die Nebenwirkungen minimieren. Abschließend erweist sich die Implantation gentechnisch modifizierter Adipozyten als neuartiger, effektiver und vielseitiger Ansatz zur Suppression von Tumorwachstum. Durch den Wettbewerb um lebenswichtige Nährstoffe im Tumormilieu kann das Fortschreiten verschiedener Krebsarten nachhaltig gebremst werden. Die Kombination aus moderner Gentechnologie, etablierten Methoden der Fettzellgewinnung und innovativen Implantationstechniken öffnet eine Tür für neue Immun- und Stoffwechseltherapien, die das Spektrum der Krebsbehandlung signifikant erweitern könnten.