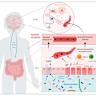
Soziale Angststörung, auch als soziale Phobie bekannt, zählt zu den häufigsten und belastendsten psychischen Erkrankungen weltweit. Betroffene leiden unter intensiver Angst vor sozialen Situationen, die ihre Lebensqualität erheblich einschränkt und oft zu Rückzug und Isolation führt. Trotz bestehender Therapiemöglichkeiten bestehen weiterhin große Herausforderungen bei der Behandlung, da die genauen biologischen Ursachen bislang nur unzureichend verstanden sind. Neue Forschungen geben jedoch Hoffnung, indem sie den Fokus auf die Rolle der Darmmikrobiota als einflussreichen Faktor bei der Entstehung und Aufrechterhaltung sozialer Ängste richten. Hierbei handelt es sich um die Gemeinschaft von Milliarden von Mikroorganismen, die im menschlichen Darm leben und weitreichende Auswirkungen nicht nur auf die Verdauung, sondern auch auf das Nervensystem und das Verhalten haben.
Der Zusammenhang zwischen Gehirn und Darm, häufig als Darm-Hirn-Achse bezeichnet, ist ein komplexes Netzwerk aus biochemischen Signalen, das über das Nervensystem, hormonelle Regelkreise und Immunmechanismen funktioniert. Es hat sich gezeigt, dass Veränderungen in der Zusammensetzung der Darmflora Auswirkungen auf das zentrale Nervensystem haben können. Bei Patienten mit sozialer Angststörung wurde eine charakteristische Veränderung des Mikrobioms festgestellt, die sich durch ein Ungleichgewicht bestimmter mikrobakterieller Gruppen auszeichnet. Forschungen, die im Jahr 2023 veröffentlicht wurden, konnten anhand von Tiermodellen demonstrieren, dass die Übertragung der Mikrobiota von Menschen mit sozialer Angststörung auf Mäuse eine spezifische Verstärkung sozialer Ängste bei den Tieren hervorrief. In dieser Studie wurde das Mikrobiom durch Stuhlproben von Patienten mit sozialer Angststörung und gesunden Kontrollpersonen sequenziert und anschließend auf keimfreie Mäuse transplantiert.
Während die Tiere mit dem Mikrobiom gesunder Probanden normales Sozialverhalten zeigten, reagierten die mit dem Mikrobenprofil der Angstpatienten besiedelten Mäuse mit einer ausgeprägten sozialen Furcht. Interessanterweise waren andere Verhaltensweisen wie allgemeine Angst und depressive Symptome nicht verändert, was auf eine spezifische Wirkung auf soziale Ängste hinweist. Diese Ergebnisse legen nahe, dass bestimmte mikrobielle Gemeinschaften maßgeblich das Verhalten in sozialen Kontexten beeinflussen können. Ein wichtiger Aspekt der Untersuchung war die Analyse des Immunsystems und hormoneller Signale im Gehirn der behandelten Mäuse. Es zeigte sich, dass neben den Verhaltensveränderungen auch zentrale und periphere Immunfunktionen beeinträchtigt waren.
Zudem wurde eine veränderte Expression von Oxytocin im Bereich des sogenannten Kerns des Stria terminalis festgestellt – einem Hirnareal, welches stark mit emotionalen und sozialen Verarbeitungsprozessen verbunden ist. Oxytocin gilt als sogenanntes „soziales Hormon“ und moduliert Vertrauen, Bindung und Angstverhalten. Die Studie weist darauf hin, dass das Mikrobiom über Immunmodulation und neuroendokrine Signalwege die Oxytocinaktivität beeinflussen und somit soziale Angstreaktionen verändern kann. Diese Erkenntnisse sind wegweisend für das Verständnis der biologischen Grundlagen sozialer Angststörungen. Sie eröffnen neue Perspektiven für innovative Therapiemethoden, die gezielt das Darmmikrobiom adressieren könnten, um soziale Ängste zu lindern.
Bisherige Behandlungsmöglichkeiten basieren überwiegend auf Psychotherapie, etwa kognitiver Verhaltenstherapie, und medikamentösen Ansätzen wie Antidepressiva oder Anxiolytika. Die Integration von Mikrobiom-basierten Interventionen stellt eine Ergänzung dar, die möglicherweise nebenwirkungsärmer und nachhaltiger wirken kann. Konkrete Anwendungen könnten Probiotika, präbiotische Nahrungsmittel oder sogar fäkale Mikrobiota-Transplantationen umfassen, um das Gleichgewicht der Darmbakterien wiederherzustellen. Allerdings stehen noch viele Fragen offen, wie genau einzelne Bakterienarten oder deren Stoffwechselprodukte auf das Gehirn wirken, welche mikrobielle Profile mit welchen Symptomen korrelieren und wie sich individuelle Unterschiede in Genetik und Umweltfaktoren auf diese Zusammenhänge auswirken. Weitere klinische Studien am Menschen sind notwendig, um die Übertragbarkeit der Tiermodellergebnisse zu bestätigen und sichere sowie effektive Behandlungsprotokolle zu entwickeln.
Neben der medizinischen Relevanz unterstreicht die Forschung die Bedeutung von Ernährung und Lebensstil für psychische Gesundheit. Eine vielfältige und ausgewogene Ernährung, die reich an Ballaststoffen, fermentierten Lebensmitteln und wenig stark verarbeiteten Produkten ist, fördert eine gesunde Mikrobiota. Stressmanagement, Bewegung und ausreichender Schlaf tragen ebenfalls dazu bei, das Gleichgewicht der Darmflora zu stabilisieren und so möglicherweise soziale Ängste positiv zu beeinflussen. In der gesellschaftlichen Wahrnehmung rückt das Thema psychische Erkrankungen zunehmend in den Mittelpunkt. Die Akzeptanz und das Verständnis für Betroffene wachsen und fördern eine bessere Unterstützung im Alltag.


![The Most Hardcore Railroad Crossing [video]](/images/455C11A2-4359-495A-BB26-90633F34CCC8)