Die Erforschung komplexer Krankheiten wie Diabetes, Krebs oder Asthma stellt Wissenschaftler seit Jahrzehnten vor enorme Herausforderungen. Im Gegensatz zu einfachen genetischen Erkrankungen, die durch einzelne Genmutationen verursacht werden, sind komplexe Krankheiten das Ergebnis eines Zusammenspiels vieler Gene. Das macht es schwierig, die spezifischen Genkombinationen zu identifizieren, die letztendlich für die Entstehung solcher Krankheiten verantwortlich sind. Doch ein bahnbrechender Fortschritt in diesem Bereich wurde nun durch den Einsatz künstlicher Intelligenz erzielt – eine Entwicklung, die potenziell die Diagnose- und Behandlungsmöglichkeiten revolutionieren könnte. Forscher der Northwestern University haben eine neuartige computergestützte Methode entwickelt, die anhand von begrenzten Genexpressionsdaten die entscheidenden Genkombinationen erkennt, die komplexen Krankheiten zu Grunde liegen.
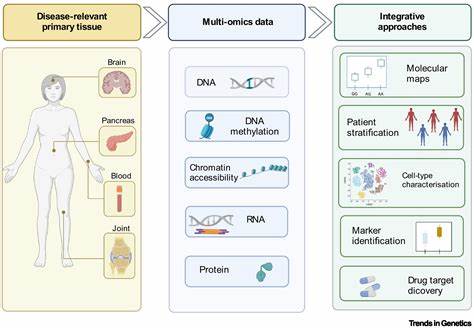
Im Gegensatz zu herkömmlichen Herangehensweisen, die oft einzelne Gene isoliert betrachten, nutzt dieses Verfahren generative KI-Modelle, um Muster kollektiver Genaktivität zu entschlüsseln. Es zeigt damit auf, wie mehrere Gene in Netzwerken zusammenwirken, um Eigenschaften oder Krankheitszustände hervorzubringen. Das innovative Modell mit dem Namen Transcriptome-Wide conditional Variational auto-Encoder (kurz TWAVE) stellt eine Verbindung zwischen maschinellem Lernen und Optimierungsmethoden her, um die Mechanismen von Genexpression besser zu verstehen. Es fokussiert dabei nicht auf die reine DNA-Sequenz, sondern auf die tatsächliche Genexpression, also die Aktivität der Gene in Zellen. Dieser Ansatz ist besonders wichtig, da sich die Genexpression dynamisch verändert und durch Umweltfaktoren, Lebensstil sowie andere Einflüsse moduliert wird.
Ein besonderer Vorteil der Analyse der Genexpression liegt darin, dass sie eine Art Momentaufnahme der zellulären Aktivität liefert, die über reine genetische Informationen hinausgeht. Während DNA-Daten hochgradig persönlich und potenziell sensibel sind, ermöglicht Genexpressionsdaten eine effektivere und dennoch datenschutzfreundlichere Analyse. Zudem können Umwelteinflüsse, die in der DNA nicht erfasst werden, auf diese Weise indirekt berücksichtigt werden. Die Forscher trainierten das KI-Modell mit umfangreichen Daten aus klinischen Studien, in denen die Genexpressionsprofile von gesunden und kranken Probanden erfasst wurden. So konnte TWAVE lernen, die Muster zu unterscheiden, die mit Krankheitsbildern einhergehen.
Mithilfe eines Optimierungsmechanismus identifiziert das Modell zudem jene Genveränderungen, die am ehesten dazu führen, dass eine Zelle vom gesunden in den krankhaften Zustand übergeht – und umgekehrt. Die Ergebnisse sind beeindruckend. TWAVE gelang es, krankheitsverursachende Genkombinationen aufzudecken, die bisherige Methoden nicht erkennen konnten. Darüber hinaus zeigte sich, dass unterschiedliche Genkombinationen bei verschiedenen Patienten zu ähnlichen klinischen Erscheinungsbildern führen können. Dieser Befund unterstreicht die Bedeutung personalisierter Medizin, bei der Therapieansätze individuell auf die genetischen Profile jedes Patienten zugeschnitten werden.
Dieser Fortschritt bietet enorme Chancen für die Entwicklung neuer, multi-target Therapeutika. Statt sich nur auf einzelne Gene zu konzentrieren, ermöglichen die Erkenntnisse eine ganzheitliche Sicht auf die genetischen Netzwerke, wodurch Therapien effizienter und gezielter gestaltet werden können. Die Komplexität, die einst als unüberwindbares Hindernis galt, wird durch den Einsatz fortschrittlicher KI-Technologie beherrschbar gemacht. Der studierte Physiker Adilson Motter, dessen Arbeitsgruppe diese Forschung leitete, vergleicht komplexe Krankheiten gern mit einem Flugzeugabsturz. Dabei sind nicht einzelne Fehler ausschlaggebend, sondern das Zusammenspiel mehrerer Pannen, die zu einer Katastrophe führen.
Ebenso tragen bei Erkrankungen oft mehrere genetische „Fehler“ oder Veränderungen zum Ausbruch der Krankheit bei. Das KI-Modell hilft, diese komplexen Zusammenhänge aufzudecken – eine Leistung, die frühere statistische Methoden aufgrund der Vielzahl möglicher Genkombinationen nicht erzielen konnten. Die Relevanz dieser Erkenntnisse geht weit über die Gesundheitsforschung hinaus. Sie zeigt, wie leistungsfähig künstliche Intelligenz in der Analyse biologischer Systeme sein kann und ebnet den Weg für eine neue Ära der biomedizinischen Forschung. Die Möglichkeit, präzise festzustellen, welche Genaktivitäten für welche Krankheitsbilder verantwortlich sind, wird die Entwicklung neuer diagnostischer Werkzeuge und Therapien fördern.
Darüber hinaus wird die Integration von Umweltfaktoren in die Genexpressionsanalyse die Forschung zu Krankheitsursachen erweitern. Die Wechselwirkung von Genen und Umwelt war lange Zeit schwer zu quantifizieren, nun lassen sich diese komplexen Dynamiken besser nachvollziehen. Damit wird es auch möglich, personalisierte Vorbeugungsstrategien zu entwickeln, die nicht nur auf genetische Risiken, sondern auch auf Umwelt- und Lebensstilfaktoren reagieren. Die Auswirkungen dieser Forschung sind sowohl für Patienten als auch für das Gesundheitssystem enorm. Individuell zugeschnittene Therapieansätze werden voraussichtlich wirksamer sein und unerwünschte Nebenwirkungen reduzieren.
Zudem könnten dadurch Behandlungskosten langfristig gesenkt werden, da ineffektive oder allgemeine Therapien weniger genutzt werden müssen. Die Entwicklung von TWAVE wurde mit Unterstützung renommierter Institutionen wie dem National Cancer Institute und der National Science Foundation vorangetrieben. Die daraus resultierende Studie wurde im Juni 2025 in den Proceedings of the National Academy of Sciences veröffentlicht, was die hohe wissenschaftliche Anerkennung unterstreicht. In der Zukunft könnte diese Technologie auch für andere komplexe Merkmale – etwa intellektuelle Leistungen oder physische Eigenschaften – relevant sein. Denn auch diese Eigenschaften entstehen aus der komplexen Interaktion vieler Gene und deren Ausdrucksmuster.
Somit bietet das Konzept eine Plattform, um sowohl medizinische als auch biologische Fragestellungen auf eine neue Art zu erforschen. Zusammenfassend stellt die Verwendung von KI zur Analyse von Genexpressionsdaten einen Paradigmenwechsel in der genetischen Forschung dar. Sie ermöglicht es, die genetischen Netzwerke hinter Krankheiten zu verstehen und gezielt zu beeinflussen. Dies ist ein bedeutender Schritt hin zu besserer medizinischer Versorgung und individualisierter Therapie, die auf den einzigartigen genetischen und umweltbedingten Bedingungen jedes Einzelnen basieren. Die Zukunft der Medizin wird maßgeblich von solchen innovativen Ansätzen bestimmt werden, die interdisziplinäres Wissen aus Physik, Informatik, Biologie und Medizin vereinen.
Die Ergebnisse der Northwestern University zeigen eindrucksvoll, wie künstliche Intelligenz komplexe biologische Fragestellungen lösen kann und damit neue Horizonte für die Bekämpfung von Krankheiten eröffnet.