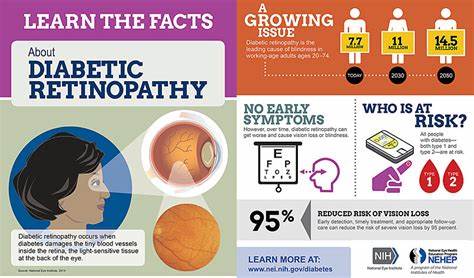
Die diabetische Retinopathie (DR) zählt zu den häufigsten Komplikationen des Diabetes mellitus und ist eine der Hauptursachen für vermeidbare Erblindungen weltweit. Früherkennung und regelmäßiges Screening sind entscheidend, um Behandlungen rechtzeitig einzuleiten und den Krankheitsverlauf günstig zu beeinflussen. In diesem Kontext gewinnt die nicht-mydriatische digitale Retinographie als minimalinvasive und patientenfreundliche Screening-Methode zunehmend an Bedeutung. Noch innovativer und vielversprechender gestaltet sich der Einsatz künstlicher Intelligenz (KI) zur Unterstützung oder Automatisierung der Bildauswertung in der Retinographie. Dieser Wandel bringt neue Chancen, stellt aber auch Herausforderungen in der klinischen Nutzung und Bewertung dar.
Unter nicht-mydriatischer Retinographie versteht man die Erstellung von Netzhautbildern ohne medikamentös ausgelöste Erweiterung der Pupille. Dies ermöglicht eine einfachere und zeitsparendere Untersuchung, die vor allem in der Primärversorgung und in ländlichen oder ressourcenarmen Regionen häufig eingesetzt wird. Allerdings kann die Bildqualität durch fehlende Pupillenerweiterung limitiert sein, was die Diagnose erschwert. Hier setzen KI-gestützte Verfahren an, die mittels Deep-Learning-Algorithmen und großen Bilddatenbanken trainiert wurden, um trotz verschiedener Bildqualitäten zuverlässige Befunde zu generieren. In der klinischen Praxis sind bei der Erkennung der diabetischen Retinopathie insbesondere zwei diagnostische Parameter relevant: die Sensitivität, also die Fähigkeit, wirklich alle betroffenen Patienten zu erkennen, und die Spezifität, also die Vermeidung von falsch-positiven Befunden.
Aktuelle wissenschaftliche Übersichtsarbeiten zeigen, dass KI-Systeme bei der Erkennung von zumindest behandlungsbedürftiger DR hohe Sensitivitätswerte von bis zu 100 % erreichen können. Die Spezifität hingegen variiert stärker und liegt in Studien zwischen 20 % und nahezu 100 %. Diese Schwankungen sind häufig auf Unterschiede in den verwendeten Kameratypen, Algorithmen, Studienpopulationen und Qualitätsstandards zurückzuführen. Eine wichtige Kennzahl zur Beurteilung der diagnostischen Gesamtleistung ist der sogenannte AUROC-Wert (Area Under the Receiver Operating Characteristic Curve). Werte zwischen 0,9 und 1,0 signalisieren eine exzellente Erkennungsrate.
In der Anwendung von KI in der nicht-mydriatischen Retinographie liegt dieser Wert typischerweise zwischen 0,88 und 0,99, was auf eine sehr hohe Genauigkeit hindeutet. Besonders die frühen Stadien der diabetischen Retinopathie, die für eine rechtzeitige Intervention entscheidend sind, können damit zuverlässig detektiert werden. Die Integration von KI in die Retinologie ist jedoch kein Selbstläufer. Die Heterogenität der verfügbaren Softwares und Hardwarekomponenten erfordert eine sorgfältige Auswahl und Validierung vor Ort. Manche KI-Systeme wurden auf Bildern von mydriatischen Kameras trainiert und erzielen möglicherweise schlechtere Ergebnisse bei nicht-mydriatischen Aufnahmen.
Ebenso kann die Komplexität der DR-Befunde, wie mikrovaskuläre Veränderungen, Makarödem oder proliferative Veränderungen, die Algorithmen vor Herausforderungen stellen. Eine einheitliche Standardisierung der Datenqualität sowie der Evaluationsmethoden ist erforderlich, um den klinischen Nutzen nachhaltig zu sichern. Darüber hinaus fehlt es aktuell noch an ausreichend hochwertigen Studien bezüglich der klinischen Effektivität und Sicherheit der KI-gestützten Screening-Methoden. Viele vorhandene systematische Übersichtsarbeiten sind von niedriger Qualität, was die Evidenzlage limitiert. Um die Anwendung von KI im Alltag zu fördern, bedarf es weiterer Forschung, die prospektiv Erfolge, Risiken sowie Kosten-Nutzen-Aspekte umfassend untersucht.
Nicht-mydriatische digitale Retinographie mit KI-Unterstützung erlaubt zudem eine praktikable Entlastung des medizinischen Fachpersonals. Automatisierte Bildbewertungen ermöglichen schnellere Diagnoseentscheidungen und eine effizientere Steuerung von Follow-up-Untersuchungen. Besonders in Gebieten mit eingeschränktem Zugang zu spezialisierten Augenärzten kann dies die Versorgungsqualität deutlich verbessern. Dadurch eröffnet sich die Möglichkeit, durch telemedizinische Vernetzung größere Bevölkerungsgruppen zu screenen und so die Früherkennung von diabetischer Retinopathie weltweit zu verbreiten. Die Digitalisierung und die Analyse großer Datenmengen eröffnen aber auch datenschutzrechtliche Herausforderungen.
Die Verarbeitung sensibler Gesundheitsdaten mittels KI-Systemen erfordert die Einhaltung strenger Datenschutzrichtlinien. Zudem sind Transparenz, Nachvollziehbarkeit der Algorithmusentscheidungen und die Qualifikation des medizinischen Personals für den Umgang mit KI von zentraler Bedeutung, um ethische und rechtliche Anforderungen zu erfüllen. Neben der reinen Diagnoseunterstützung werden KI-Modelle zunehmend für die Klassifikation von Krankheitsstadien, die Prognoseabschätzung und die Personalisierung der Therapie eingesetzt. So könnte in Zukunft automatisiert bestimmt werden, welche Patienten von einer intensiveren augenärztlichen Betreuung profitieren oder wann Lasertherapie beziehungsweise intravitreale Injektionen angezeigt sind. Die Verbindung dieser Funktionen in einem integrierten Versorgungssystem verspricht eine ganzheitliche Optimierung in der Diabetesversorgung.
Aus Perspektive von Gesundheitspolitik und Regulierungsbehörden ist es wichtig, die Auswahl und Zulassung von KI-basierten Screening-Tools sorgfältig zu kontrollieren. Nur durch validierte, evidenzbasierte und sichere Systeme kann das Vertrauen von Anwendern und Patienten gestärkt werden. Gleichzeitig sollte der Zugang zu dieser Technologie auch für weniger privilegierte Gesundheitssysteme gewährleistet sein, um globale Versorgungsunterschiede zu verringern. Zusammenfassend lässt sich sagen, dass künstliche Intelligenz in der nicht-mydriatischen digitalen Retinographie eine vielversprechende Innovation zur Verbesserung des Screenings bei diabetischer Retinopathie darstellt. Die aktuellen Ergebnisse sind zwar vielversprechend, doch bleiben Herausforderungen bei der Standardisierung, Validierung sowie der angesichts der unterschiedlichen Geräte und Algorithmen bestehenden Heterogenität bestehen.
Die Zukunft der retinalen Diagnostik wird maßgeblich davon abhängen, wie KI in die etablierten klinischen Pfade eingebunden wird und wie hochwertige, aktuell verfügbare Evidenz genutzt wird, um patientenzentrierte Versorgung zu verbessern. Es ist zu erwarten, dass die kontinuierliche Weiterentwicklung von KI-Algorithmen und die Verbesserung digitaler Retinographiekameras die Sensitivität und Spezifität weiter steigern werden. Damit verbunden sind Chancen für eine breitere und kosteneffektivere Bevölkerungsüberwachung. Für Ärzte, Patienten und Gesundheitssysteme bietet dies eine neue Qualität der Vorsorge und Behandlung, die langfristig Sehverlust durch Diabetes wirksam reduzieren kann.