In den letzten Jahren hat die Wissenschaft immer mehr Verständnis dafür gewonnen, wie Aminosäuren, die Bausteine von Proteinen, den menschlichen Stoffwechsel beeinflussen. Besonders der Zusammenhang zwischen bestimmten Aminosäuren und dem Körpergewicht rückt zunehmend in den Fokus der Forschung. Eine herausragende Rolle spielt dabei die Aminosäure Cystein. Neue Studien, insbesondere Untersuchungen an Mäusen, zeigen, dass ein Mangel an Cystein zu einem außergewöhnlich schnellen und nachhaltigen Gewichtsverlust führen kann. Doch wie hängt dieser Prozess genau zusammen und welche Mechanismen liegen dem zugrunde? Cystein ist eine schwefelhaltige Aminosäure, die in vielen biologischen Prozessen unverzichtbar ist.
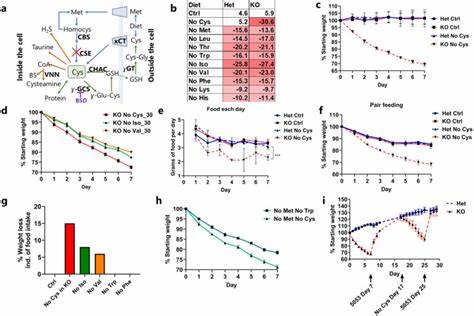
Obwohl sie im Gegensatz zu anderen Aminosäuren als semi-essentiell gilt, da der Körper sie über Methionin synthetisieren kann, ist ihre Verfügbarkeit entscheidend für die Gesundheit. Besonders bei genetischen Defekten im Transsulfurierungsweg, der für die Synthese von Cystein aus Methionin zuständig ist, wird Cystein essentiell. Die kritische Bedeutung von Cystein zeigt sich auch darin, dass ein Defizit dieser Aminosäure bei Mäusen, die eine genetische Disposition für eingeschränkte Cysteinsynthese haben, zu einem dramatischen Gewichtsverlust von bis zu 30 Prozent innerhalb einer Woche führt. Die Forschung konzentrierte sich auf die Auswirkungen des Entzugs einzelner essentieller Aminosäuren aus der Ernährung von Mäusen. Dabei wurde deutlich, dass kein anderer Aminosäuremangel einen so ausgeprägten Gewichtsverlust verursacht wie der Mangel an Cystein.
Dies geschieht unabhängig von der Kalorienaufnahme allein, denn der Gewichtsverlust übersteigt deutlich den Effekt, der durch eine reduzierte Nahrungskarenz erklärt werden könnte. Somit steht fest, dass Cystein eine einzigartige Rolle im Metabolismus einnimmt. Was passiert auf molekularer Ebene bei Cysteinmangel? Die Zellen aktivieren eine sogenannte integrierte Stressantwort, eine Schutzreaktion auf Aminosäurenknappheit. Dabei wird der Signalweg des Proteins GCN2 stimuliert, der durch unbeladene tRNA-Moleküle aktiviert wird, was wiederum zur Phosphorylierung des Initiationsfaktors eIF2α führt. Diese Phosphorylierung hemmt generell die Proteinsynthese, fördert jedoch die Translation bestimmter Gene, darunter den Transkriptionsfaktor ATF4.
ATF4 aktiviert verschiedene Gene, die an Stressreaktionen beteiligt sind, insbesondere GDF15 und FGF21, zwei Hormone, die eine bedeutende Rolle bei der Regulation von Appetit, Energiestoffwechsel und Körpergewicht spielen. Das Zusammenspiel dieser Signalmoleküle erklärt zum Teil die beobachteten Effekte des schnellen Gewichtsverlusts. Darüber hinaus spielt Cystein eine wesentliche Rolle in der Synthese von Glutathion (GSH), einem lebenswichtigen antioxidativen Molekül, das die Zelle vor oxidativem Stress schützt. Ein Mangel an Cystein führt zu einer Reduktion von GSH, was wiederum zu einer Aktivierung des oxidativen Stressantwortsystems über den Transkriptionsfaktor NRF2 führt. Das Zusammenwirken von integrierter Stressreaktion und oxidativem Stress verstärkt die metabolischen Auswirkungen und entzieht dem Körper wichtige Schutzmechanismen.
Ein überraschender Befund der Untersuchungen ist die starke Abnahme des Gehalts an Coenzym A (CoA) in den Geweben bei Cysteinmangel. CoA ist ein zentraler Metabolit im Energiestoffwechsel, insbesondere in der mitochondrialen Funktion, wo es an der Energiefreisetzung aus Fettsäuren und Kohlenhydraten beteiligt ist. Obwohl CoA bislang als extrem stabil galt und selbst bei Mangel an Pantothensäure (Vitamin B5) kaum abgebaut wird, zeigt sich beim Cysteinmangel eine erhebliche Verringerung der CoA-Spiegel. Diese Abnahme führt zu einer reduzierten Funktionalität der Mitochondrien und verursacht eine Umbewertung des Energiestoffwechsels: Die Mitochondrien verarbeiten Energiesubstrate weniger effizient, die Tricarbonsäurezyklusfunktion ist eingeschränkt und die Energiegewinnung verlagert sich zugunsten der ineffizienten anaeroben Glykolyse. Die Konsequenz dieses metabolischen Umschaltens ist eine vermehrte Ausscheidung von Zwischenprodukten des Stoffwechsels über den Urin, wie Pyruvat, Citrate und α-Ketoglutarat, die nicht vollständig von den Zellen verarbeitet werden können.
Dieser Prozess stellt eine Energieverschwendung dar, die zusätzlich zum Gewichtsverlust beiträgt. Gleichzeitig beobachten die Forschenden eine verstärkte Lipolyse – also den Abbau von Fettdepots – und eine braune Umwandlung des weißen Fettgewebes, die thermogenetische Aktivität anregt und den Kalorienverbrauch erhöht. Ein besonders bemerkenswerter Aspekt der Cysteinmangel-bedingten Effekte ist die schnelle Wiederherstellbarkeit. Sobald Cystein wieder in der Nahrung zugeführt wird, gewinnen die Mäuse innerhalb weniger Tage einen Großteil des verlorenen Gewichts zurück. Diese hohe Reversibilität legt nahe, dass die durch Cysteinmangel induzierten Effekte ein adaptives metabolisches Programm sind, das dem Organismus ermöglicht, auf spezifische ernährungsbedingte Stresssituationen zu reagieren.
Die wissenschaftliche Aufmerksamkeit für die Rolle von Aminosäuren in der Gewichtsregulation wächst stetig. Während die Beschränkung bestimmter Aminosäuren, zum Beispiel Methionin oder verzweigtkettiger Aminosäuren (BCAAs), bereits als mögliche Strategie zur Verbesserung der metabolischen Gesundheit diskutiert wird, rücken nun die einzigartigen Auswirkungen des Cysteins in den Vordergrund. Im Vergleich zu anderen essentiellen Aminosäuren führt Cysteinmangel nicht nur zu Gewichtsreduktion durch Energieabschöpfung und Appetitminderung, sondern auch zu bedeutsamen Veränderungen im zellulären Energiehaushalt. Diese Erkenntnisse eröffnen neue Perspektiven für therapeutische Interventionen bei Adipositas und stoffwechselbedingten Erkrankungen. Die Möglichkeit, gezielt den Cysteinstatus zu regulieren, um einen kontrollierten Gewichtsverlust zu erzielen, ist spannend.
Zugleich erfordern die potenziellen Risiken, wie etwa oxidative Schäden durch gestörte Glutathionsynthese oder metabolische Dysbalancen durch reduzierte CoA-Verfügbarkeit, eine sorgfältige Abwägung. Neben der möglichen Anwendung in der Medizin liefern die Studien auch wichtige Hinweise für die Ernährungswissenschaft. Die Versorgung mit Cystein und Methionin sollte bei verschiedenen Bevölkerungsgruppen, insbesondere solchen mit genetischen oder metabolischen Einschränkungen, genau beobachtet werden. Zudem könnten personalisierte Ernährungsansätze entwickelt werden, die den Aminosäuregehalt gezielt an den individuellen Stoffwechsel anpassen, um Effektivität und Sicherheit der Diätstrategien zu maximieren. Bemerkenswert ist, dass neben der metabolischen Umprogrammierung des Organismus auch die Aktivierung hormoneller Signalwege eine Rolle spielt.
Die Anhebung der Glutendermüllhormone GDF15 und FGF21 wirkt appetitzügelnd und beeinflusst den Energieverbrauch – ein System, das evolutionär vermutlich dazu dient, den Organismus bei Nährstoffmangel vor Schaden zu schützen. Die Tatsache, dass die Eliminierung oder Reduktion dieser Hormone die Gewichtsabnahme verringert, unterstreicht ihre zentrale Funktion. Die komplexen Interaktionen zwischen Nahrung, Stoffwechsel und Hormonhaushalt verdeutlichen, wie sensibel der Körper auf einzelne Aminosäuren reagiert und wie solche Ernährungskomponenten die Gesundheit weitreichend beeinflussen können. Die zugrunde liegenden Mechanismen, wie die integrierte Stressantwort, die antioxidative Abwehr und die Koordination der Energieproduktion in den Mitochondrien, sind von fundamentaler Bedeutung für das Verständnis von Altersprozessen, Stoffwechselstörungen und potenzieller Langlebigkeit. Abschließend lässt sich sagen, dass der schnelle Gewichtsverlust im Zusammenhang mit Cysteinmangel eine vielschichtige physiologische Reaktion darstellt, die auf molekularen, zellulären und systemischen Ebenen wirkt.