Schlangenbisse stellen nach wie vor ein gewaltiges, meist unterschätztes Gesundheitsproblem dar. Weltweit verursachen sie jährlich weit über hunderttausend Todesfälle und führen bei Hunderttausenden weiteren Menschen zu bleibenden Behinderungen. Besonders in tropischen und subtropischen Regionen mit begrenztem Zugang zur medizinischen Versorgung sind diese Zahlen alarmierend hoch. In Anbetracht dieser Herausforderung arbeiten Wissenschaftler kontinuierlich an verbesserten Therapien, die sowohl sicherer als auch effektiver sind. Aktuell zeigt sich, dass eine Kombination aus dem kleinen Molekül Varespladib und neutralisierenden menschlichen Antikörpern ein vielversprechender Ansatz zur Behandlung von Schlangengiftvergiftungen ist.
Traditionell basieren die meisten verfügbaren Antivenome auf tierischen Polyclonalantikörpern, welche durch Immunisierung von Pferden oder Schafen gewonnen werden. Diese Produkte haben jedoch mehrere Nachteile: Oftmals ist ihre Wirkung nur auf bestimmte Schlangengattungen oder -arten begrenzt, Nebenwirkungen wie allergische Reaktionen sind häufig, und die Produktionsprozesse sind teuer und zeitaufwendig. Dazu kommt, dass viele Schlangengifte hochvariabel zusammengesetzt sind und mit bisherigen Antivenomen oft nicht ausreichend neutralisiert werden können. Die Suche nach einer effizienten, breit wirksamen Behandlung war daher ein wichtiger Antrieb für die Forschung.Hier setzt der innovative Cocktail aus Varespladib und neutralisierenden menschlichen Antikörpern an.
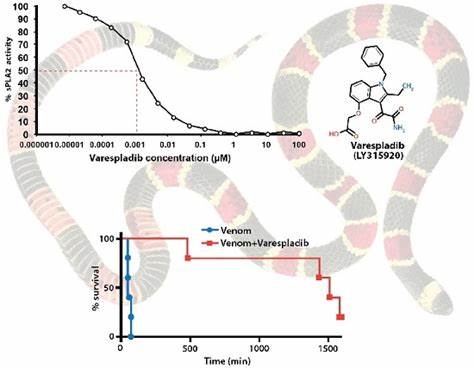
Varespladib ist ein stark wirkender Inhibitor der sekretorischen Phospholipase A2 (PLA2), einem Enzym, das in vielen Schlangengiften in großer Menge vorkommt und für toxische Wirkungen wie Zellzerstörung, Entzündung und Gewebeschädigung verantwortlich ist. Durch die Hemmung der PLA2-Funktion kann Varespladib also einen bedeutenden Teil der pathologischen Prozesse von Schlangengiften blockieren, was die Überlebenschancen von Betroffenen deutlich verbessert. Klinische und präklinische Studien haben bereits die Wirksamkeit von Varespladib gegen eine Vielzahl von Schlangengiften belegt, was es zu einer universellen Basis für die Antivenom-Entwicklung macht.Doch Schlangengifte bestehen meist aus einem komplexen Gemisch verschiedener Toxine. Neben PLA2 kommen vor allem neurotoxische Proteine wie dreifingrige Neurotoxine (Three-Finger Toxins, 3FTx) vor, die die neuromuskuläre Signalweiterleitung stören und zu lebensbedrohlicher Lähmung führen können.
Diese Neurotoxine zu neutralisieren, stellt eine große Herausforderung dar, da sie hochvariabel und in ihrer Produktion aufwändig sind. Genau hier kommen die neutralisierenden menschlichen Antikörper ins Spiel. Diese Antikörper wurden aus dem Gedächtnis-B-Zell-Repertoire eines hyperimmunisierten menschlichen Spenders isoliert, der eine langjährige Exposition gegenüber verschiedenen Schlangengiften hatte. Durch moderne molekularbiologische Verfahren ist es gelungen, Antikörper zu identifizieren, die breit gegen konservierte funktionelle Bereiche der Neurotoxine wirken und so eine umfassende Neutralisation gewährleisten.Die Kombination der zwei Technologien – Varespladib als breit wirksamer chemischer Inhibitor der PLA2-Toxine und die spezifisch neutralisierenden menschlichen Antikörper gegen Neurotoxine – ergibt einen dreifach wirksamen Cocktail, der in Versuchen mit 19 verschiedenen elapiden Schlangenarten, die von der Weltgesundheitsorganisation (WHO) als besonders gefährlich eingestuft werden, eine nahezu vollständige Schutzwirkung zeigte.
Diese Tiere überlebten selbst nach der Verabreichung ganzer Venendosen, die sonst tödlich wären, was neue Hoffnungen für die medizinische Behandlung von Schlangenbissen eröffnet.Die Mechanismen hinter der Wirkung der neutralisierenden menschlichen Antikörper sind faszinierend und hochspezifisch. Durch kristallographische Studien konnte gezeigt werden, dass diese Antikörper die gleichen Bindungsstellen auf den Neurotoxinen nutzen wie die natürlichen Rezeptoren in menschlichen Nervenzellen, insbesondere den nikotinischen Acetylcholinrezeptor. Dadurch verhindern die Antikörper effektiv das Andocken der Neurotoxine an ihre Zielstrukturen und blockieren so die neurotoxische Wirkung. Diese „Mimikry“ der natürlichen Ligandenbindung verleiht den Antikörpern eine herausragende Neutralisationskraft und erweitert ihre Reichweite gegenüber unterschiedlichen Toxinvarianten.
Darüber hinaus bietet das neue Therapiekonzept durch seine molekulare Definition und Humanisierung der Antikörper entscheidende Vorteile hinsichtlich Verträglichkeit und Sicherheit. Menschliche Antikörper reduzieren das Risiko immunologischer Nebenwirkungen und könnten langfristig eine präzisere und personalisierte Behandlung ermöglichen, angepasst an die in der jeweiligen Region vorherrschenden Schlangenarten und Giftzusammensetzungen.Ein weiterer relevanter Aspekt ist die Stabilität und Herstellbarkeit des Varespladib/Antikörper-Cocktails. Varespladib lässt sich als kleines Molekül kostengünstig produzieren und ist oral bioverfügbar, was in vielen Fällen die schnelle Verabreichung direkt am Ort des Bisses ermöglichen könnte. Humanisierte Antikörper können mittels moderner Biotechnologie in Zellkulturen effizient erzeugt werden und verfügen über lange Halbwertszeiten im Blut, was auch eine anhaltende Schutzeffizienz verspricht.
Die Auswirkungen dieser Forschung auf das globale Gesundheitswesen könnten enorm sein. Gerade in ländlichen Gebieten mit begrenztem Zugang zu spezialisierten Kliniken und herkömmlichem Antivenom, das häufig kühl gelagert werden muss, besteht ein großer Bedarf nach leicht handhabbaren und breit wirksamen Therapiemöglichkeiten. Eine orale oder intravenöse Gabe eines definierten Cocktail-Medikaments, das robust und breit wirksam ist, würde Behandlungszeiten und Mortalität signifikant reduzieren.Nicht zuletzt illustriert diese Entwicklung auch den Fortschritt der biologischen Forschung und medizinischen Innovation. Die Verbindung von Strukturbiologie, moderner Antikörpertechnologie und pharmakologischer Inhibitorentwicklung zeigt exemplarisch, wie interdisziplinäre Ansätze neue Wege zur Lösung jahrhundertealter Gesundheitsprobleme öffnen können.
Das gezielte Design neutralisierender Antikörper mit menschlicher Herkunft auf konservierte toxische Schnittstellen und die Ergänzung durch ein wirksames kleineres Molekül stellen den derzeit modernsten Stand der Antivenom-Forschung dar.In Zukunft sind weitergehende klinische Studien nötig, um die Sicherheit, Dosierung und Wirksamkeit unter realen Bedingungen zu prüfen. Zudem besteht Potenzial, die Palette der neutralisierenden Antikörper zu erweitern und Herausforderungen wie die Neutralisation weiterer Toxinfamilien anzugehen. Auch Kombinationen mit anderen Wirkstoffen könnten die Effektivität noch steigern.Zusammenfassend lässt sich sagen, dass die Kombination aus Varespladib und neutralisierenden menschlichen Antikörpern einen bedeutenden Durchbruch in der Therapie von Schlangenbissvergiftungen darstellt.
Sie weist den Weg zu einer möglichst sicheren, breit wirksamen und kosteneffizienten Behandlung, die viele Leben retten und bleibende Schäden verhindern kann. Damit bekommt das Thema Schlangengift eine neue Dimension in der medizinischen Forschung und verbindet innovative Biotechnologien mit lebensrettender klinischer Anwendung. Die Zukunft der Antivenom-Therapie könnte so bunter, wirksamer und zugänglicher werden als je zuvor.