Koffein ist aus dem modernen Alltag kaum mehr wegzudenken. Millionen Menschen starten ihren Tag mit einer Tasse Kaffee oder greifen zwischendurch zu koffeinhaltigen Getränken, um ihre Wachsamkeit und Leistungsfähigkeit zu steigern. Trotz seiner großen Beliebtheit und der bekannten anregenden Wirkung sind die genauen Effekte von Koffein auf das Gehirn während des Schlafs bislang noch nicht vollständig entschlüsselt. Besonders spannend sind dabei jüngste Erkenntnisse, die den Einfluss von Koffein auf die Komplexität und Kritikalität des Gehirns im Schlaf in Abhängigkeit vom Alter beleuchten. Solche Veränderungen neuronaler Dynamiken könnten weitreichende Folgen für die Schlafqualität, Erholung und psychische Gesundheit haben.
Die neurophysiologischen Grundlagen von Koffein zeigen, dass es als Adenosin-Antagonist wirkt. Adenosin ist ein körpereigener Neurotransmitter, der den Schlafdruck erhöht und somit Müdigkeit fördert. Durch die Bindung an Adenosinrezeptoren vermittelt es Erholungsprozesse des Gehirns. Koffein blockiert diese Rezeptoren, besonders die A1- und A2A-Subtypen, wodurch der natürliche Schlafreiz abgeschwächt und ein Gefühl von erhöhter Wachheit verursacht wird. Neben dieser direkten Wirkung entfacht Koffein eine Kaskade komplexer Modulationen in verschiedenen Neurotransmittersystemen, wie der Erhöhung von Dopamin- und Noradrenalinspiegeln sowie der Beeinflussung von GABA- und Glutamat-Aktivitäten.
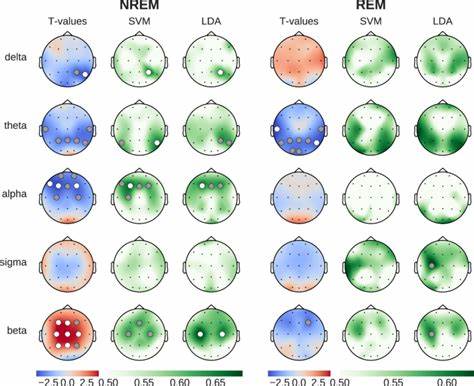
Diese Veränderungen wirken sich umfassend auf neuronale Netzwerke aus und können den Übergang zwischen Schlafstadien beeinflussen.Erste Analysen der Hirnaktivität mittels Elektroenzephalographie (EEG) zeigen, dass Koffein während des Schlafs zu spezifischen Veränderungen in den Frequenzbändern der Hirnwellen führt. So reduziert sich die Leistung langsamer Delta- und Theta-Oszillationen, die typisch für Tiefschlafphasen sind, während schnellere Beta-Frequenzen zunehmen. Interessanterweise wurden diese Effekte klarer sichtbar, als Wissenschaftler nicht nur die klassischen Frequenzbänder berücksichtigten, sondern auch die zugrundeliegende 1/f-Struktur des EEG-Signals separierten. Durch die Trennung von periodischen (rhythmischen) und aperiodischen (rauschenähnlichen) Signalanteilen konnten sie präzise feststellen, dass Koffein eine Abflachung des aperiodischen Spektrums bewirkt – ein Hinweis auf veränderte neuronale Erregungs-Inhibitions-Dynamiken.
Neben den klassischen Spektralanalysen rückt das Konzept der Gehirnkomplexität immer stärker in den Fokus der Forschung. Komplexität beschreibt das Maß der Informationsvielfalt und -verarbeitung im Gehirn. Sie kann beispielsweise mittels Entropiemethoden gemessen werden, die die Vorhersagbarkeit von neuronalen Signalen quantifizieren. Koffein erhöht während des Schlafs deutlich die Entropiewerte im EEG. Dies legt nahe, dass das Gehirn bei Koffeineinfluss in einen Zustand übergeht, in dem neuronale Aktivität vielfältiger und weniger stereotyp ist.
Besonders ausgeprägt ist dieser Effekt während der Nicht-REM-Schlafphasen – den entscheidenden Phasen der Gehirnerholung und Gedächtniskonsolidierung.Ein weiteres zentrales Konzept ist die neuronale Kritikalität. In der Neurowissenschaft bezeichnet Kritikalität einen Zustand zwischen Ordnung und Chaos, in dem das Gehirn optimal für Informationsverarbeitung und Anpassungsfähigkeit eingestellt ist. Viele Studien zeigen, dass gesunde Gehirne nahe an diesem kritischen Punkt operieren. Koffein scheint das Gehirn während des Schlafs diesem kritischen Zustand näherzubringen.
Dies spiegelt sich in der Veränderung von Messgrößen wider, die langreichweitige zeitliche Korrelationen und das Verhalten von neuronalen Netzwerken charakterisieren. Konkret sinken die Werte der detrended fluctuation analysis (DFA) sowie die Steilheit der 1/f-Komponente, die beide als Marker für eine nähere Position zum kritischen Punkt gelten.Ein besonders bemerkenswerter Befund ist, dass die Wirkung von Koffein auf Komplexität und Kritikalität altersabhängig ist. Untersuchungen zeigen, dass jüngere Erwachsene zwischen 20 und 27 Jahren einen stärkeren Anstieg der Gehirnentropie und eine ausgeprägtere Annäherung an die Kritikalität während des REM-Schlafs zeigen als Menschen mittleren Alters (41 bis 58 Jahre). Diese Altersabhängigkeit lässt sich möglicherweise auf eine Abnahme der Adenosinrezeptordichte mit zunehmendem Alter zurückführen.
Mit geringer werdender Rezeptorzahl schwächt sich die Wirkung von Koffein ab, da weniger Bindungsstellen für die Hemmung durch den Stimulator verfügbar sind. Interessanterweise sind diese Altersunterschiede in der Nicht-REM-Phase weniger ausgeprägt, was auf eine zugrundeliegende differenzierte Regulation der Schlafstadien durch Adenosin und andere Neurotransmitter hindeutet.Darüber hinaus könnten altersbedingte Veränderungen der Koffeinmetabolisierung, Schlafarchitektur und Lebensstilfaktoren die unterschiedlich starken Effekte verstärken. Ältere Menschen verarbeiten Koffein langsamer, und der Anteil sowie die Qualität des REM-Schlafs nehmen ebenfalls mit dem Alter ab, was eine geringere Störanfälligkeit durch Koffein bedingt. Somit lässt sich das Gesamtbild so interpretieren, dass jüngere Gehirne sensibler auf die stimulierenden Effekte während der tiefen, regenerativen Schlafphasen reagieren, was eventuell zu einer stärkeren Modulation der neuronalen Informationsverarbeitung führt.
Trotz der nachgewiesenen Steigerung der neuronalen Komplexität unter Koffeinbedarf gilt es zu bedenken, dass diese Zunahme auch eine Beeinträchtigung der Schlafqualität widerspiegeln könnte. Ein zu aktives Gehirn in den sonst ruhigen Schlafphasen könnte die Erholung und Normalisierung von kognitiven und physiologischen Prozessen stören. Langfristige Folgen, wie Einflüsse auf Herz-Kreislauf-, Stoffwechsel- und psychische Gesundheit, sind daher wichtige Forschungsfragen der Zukunft.Methodisch ist die Arbeit von großer Tragweite, da sie moderne Signalanalyseverfahren mit maschinellem Lernen kombiniert. Durch die Trennung von periodischen und aperiodischen Komponenten sowie die Anwendung mehrerer Entropie- und Kritikalitätsmetriken wurde eine robuste und differenzierte Abbildung der neuronalen Veränderungen möglich.
Zudem konnten auf Basis der Schlaf-EEG-Daten mittels Support Vector Machines, linearer Diskriminanzanalyse und Random Forest-Klassifikatoren die Koffein- gegen die Placebobedingung mit hoher Genauigkeit unterschieden werden. Die Merkmale der Gehirnkomplexität erwiesen sich dabei als besonders aussagekräftig, was ihre Relevanz für die Beschreibung der Wirkung von Koffein unterstreicht.Die klinische und gesellschaftliche Relevanz dieser Erkenntnisse ist erheblich. Angesichts der weit verbreiteten Koffeinexposition empfiehlt sich ein differenziertes Verständnis der Auswirkungen auf Schlaf und Gehirnfunktion. Gerade bei jüngeren Bevölkerungsgruppen, die oft auch hohen Koffeinkonsum und verkürzte Schlafzeiten kombinieren, können Beeinträchtigungen der Schlafqualität langfristige kognitive und mentale Störungen begünstigen.
Gleichzeitig zeigen neuroprotektive Eigenschaften von Koffein, etwa im Kontext von Parkinson-Erkrankungen, das ambivalente Bild dieses Stoffes.Zukünftige Forschung sollte vor allem untersuchen, inwieweit die beobachteten Veränderungen der Gehirnkomplexität und Kritikalität direkt mit kognitiven Funktionen, gesundheitlichen Parametern und subjektiven Schlafqualitätswerten korrelieren. Auch der Einfluss von chronischem versus akutem Koffeinkonsum sowie mögliche Interaktionen mit Medikamenten oder Schlafstörungen gilt es zu klären. Besonders spannend wäre die Anwendung vergleichbarer Analyseverfahren bei Patienten mit neurodegenerativen Erkrankungen, um herauszufinden, ob Koffein deren Schlaf und neuronale Dynamik ähnlich beeinflusst wie bei gesunden Probanden.Zusammenfassend lässt sich sagen, dass Koffein als psychoaktives Stimulans weitreichende altersabhängige Effekte auf die neuronale Komplexität und den kritischen Zustand des Gehirns während des Schlafs ausübt.
Diese Veränderungen bieten einen wichtigen Einblick in die Mechanismen, mit denen Koffein die Erholung und Informationsverarbeitung im Schlaf moduliert. Ein vertieftes Verständnis dieser Prozesse könnte helfen, Empfehlungen für den Koffeinkonsum besser an individuelle Bedürfnisse anzupassen und so gesundheitliche Risiken langfristig zu minimieren.