Stickstoff ist das häufigste Element in der Erdatmosphäre und bekannt für seine besonders stabile und inerteste Form, das molekulare Stickstoffgas N2. Seit langem galt die Isolation oder gar Herstellung neutraler molekularer Stickstoffallotrope jenseits von N2 als eine der größten Herausforderungen der modernen Chemie. Die extrem kurze Lebensdauer und hohe Reaktivität dieser Verbindungen machten experimentelle Nachweise nahezu unmöglich. Nun ist mit der erfolgreichen Vorbereitung des neutralen Hexanitrogens C2h-N6 ein Durchbruch gelungen, der potenziell die Entwicklung von effizienten und umweltfreundlichen Energiespeichermaterialien revolutionieren könnte. Nachfolgend wird die Entdeckung, ihre Bedeutung sowie der synthetische Weg und die Eigenschaften des neuen Moleküls umfassend dargestellt.
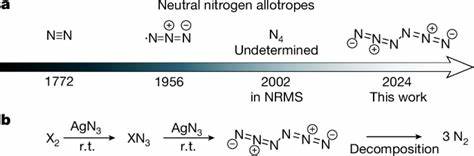
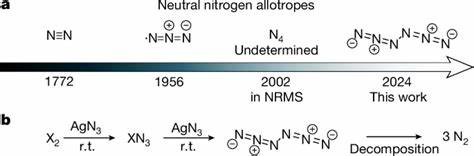
Hexanitrogen C2h-N6 ist ein neutraler polynitrogener Molekülkomplex, dessen Struktur sich deutlich von den bislang bekannten Formen wie N2 unterscheidet. Das Molekül besteht aus sechs Stickstoffatomen, die in einer offenen Kette verbunden sind und dabei keine erkennbaren N2-Einheiten bilden, was es einzigartig macht. Trotz der hohen Gesamtzahl an Elektronen und der inhärenten Schwierigkeit, stabile Verbindungen mit neutralem Stickstoff aufzubauen, zeigte sich diese Form überraschend stabil, was durch experimentelle Daten und theoretische Rechnungen bestätigt wurde. Der Schlüssel zum Erfolg der Synthese war die Reaktion zwischen Chlor- oder Bromgas mit Silberazid (AgN3) bei Raumtemperatur. Diese Reaktion, die unter reduziertem Druck durchgeführt und anschließend durch schnelles Einfrieren in Argonmatrizen bei 10 Kelvin stabilisiert wurde, ermöglichte die erstmalige Beobachtung von N6.
Die Verwendung von Argon als Matrixtestgas schützte das äußerst empfindliche Molekül vor Zersetzung und erlaubte eine detaillierte spektroskopische Analyse. Dabei konnten charakteristische Infrarot- und UV-Vis-Absorptionsbanden entdeckt werden, die in Kombination mit 15N-Isotopenmarkierungen eindeutige Hinweise auf die Existenz des Moleküls liefern. Die experimentelle Stabilität von N6 wurde zudem durch die Kondensation des neutralen Moleküls als Film bei 77 Kelvin, also bei Temperaturen von flüssigem Stickstoff, bestätigt. Solche Bedingungen sind für polynitrogene Verbindungen ungewöhnlich mild, was die Aussagekraft über die kinetische Stabilität des neuen Allotrop hervorhebt. Eine entscheidende Rolle spielte die Auswahl von AgN3 als Reagenz, da es bereits in der Synthese verschiedener Polyazide und Halogenazide erfolgreich eingesetzt wurde.
Die dabei entstehenden Zwischenprodukte und Reaktionspfade erwiesen sich als vielversprechend für die Herstellung von N6. Aus theoretischer Sicht stellte sich heraus, dass nur die trans-Konformation des C2h-symmetrischen N6-Moleküls ein energetisches Minimum auf der potenziellen Energiefläche darstellt, während andere Konformeren wie die cis-Form instabil oder reaktiv sind. Die Bindungslängen innerhalb des Moleküls sowie die Verteilung der Elektronendichte zeugen von einer Mischung aus Doppel- und Einfachbindungen, welche die Stabilität dieses exotischen Moleküls unterstützt. Analysen mit Natural Bond Orbitals zeigten darüber hinaus eine interessante Ladungsverteilung, bei der terminale Stickstoffatome neutral sind, während mittlere Atome teilweise positive und negative Ladungen tragen. Diese Verteilung begünstigt die Stabilität und erklärt das verhältnismäßig hohe Aktivierungsenergieniveau gegen Zerfall.
Die primäre Zersetzungsreaktion von N6 führt zu drei N2-Molekülen. Obwohl thermodynamisch exotherm, ist die Barriere für diesen Zerfall mit rund 14,8 Kilokalorien pro Mol hoch genug, um dem Molekül eine ausreichend lange Halbwertszeit zu verleihen, die experimentelle Studien ermöglicht. Quantenmechanische Tunneling-Effekte, die bei ähnlichen Stickstoffallotropen deren Lebensdauer drastisch verkürzen könnten, spielen hier laut Berechnungen eine untergeordnete Rolle. Dies führt zu einer abgeschätzten Halbwertszeit von über 132 Jahren bei 77 Kelvin, was den Beobachtungen konsistent entspricht. Die energetischen Eigenschaften von N6 sind überaus beeindruckend.
Bei der Zersetzung wird eine Energiefreisetzung von etwa 185 Kilokalorien pro Mol erwartet, was im Vergleich zu bekannten Sprengstoffen wie TNT oder HMX weit höher ist. Berechnungen zur Dichte des hypothetischen Kristalls prognostizieren eine gute Verdichtung mit entsprechender Detonationsgeschwindigkeit und -druck, die mehrere der gegenwärtig genutzten Hochenergieverbindungen überträffen. Damit ist N6 nicht nur ein wissenschaftliches Kuriosum, sondern potenziell auch eine Basis für zukünftige Hochleistungssprengstoffe oder Energiespeichermaterialien. Die experimentellen Methoden basierten vor allem auf der Matrixisolationsspektroskopie bei sehr tiefen Temperaturen. Dabei wurden unter kontrollierten Bedingungen die Reaktionsprodukte in Argon eingefroren und durch Infrarot- und UV-Vis-Spektroskopie analysiert.
Die Einbindung von 15N erlaubte es, durch Verschiebungen der Schwingungszustände die Strukturen der Moleküle genau zu bestimmen. Besonders die Bestätigung der verschiedenen Isotopomere mit erwarteten Intensitätsverhältnissen untermauert die Identifikation von N6. Neben der experimentellen Arbeit wurden umfangreiche Computermethoden, wie Coupled-Cluster-Berechnungen und Dichtefunktionaltheorie, zur Verfügung gestellt, um sowohl Struktur als auch Stabilität zuverlässig zu beschreiben. Die Entdeckung von neutralem Hexanitrogen C2h-N6 markiert einen Meilenstein in der polynitrogenen Chemie, weil sie die bisherige Annahme widerlegt, dass höhere neutrale molekulare Stickstoffallotrope extrem kurzlebig und praktisch unzugänglich sind. Abgesehen von geladenen polynitrogenen Anionen und Kationen, die seit einiger Zeit bekannt sind, ist dies die erste experimentelle Synthese eines neutralen Moleküls jenseits von N2 mit signifikanter Lebensdauer.
Diese Substanz erweitert das Verständnis der chemischen Bindungen im reinen Stickstoffbereich und eröffnet neue Perspektiven für Materialwissenschaften und nachhaltige Energiespeicher. Die sichere Handhabung und Synthese von Hexanitrogen bleibt eine Herausforderung, da Ausgangsmaterialien wie Silberazid und Halogenazide explosiv und gefährlich sind. Sorgfältige Laborbedingungen und spezielle Schutzmaßnahmen sind daher unerlässlich. Dennoch zeigt die beschriebene Methodik, dass die Herstellung neutraler polynitrogener Moleküle außerhalb extremer Hochdruck- oder Hochtemperaturbedingungen möglich ist. Blickt man in die Zukunft, bieten sich zahlreiche spannende Forschungsfelder.
Zum einen ist die weitere Untersuchung der physikalischen Eigenschaften von N6 in kondensierter Form oder als Komposit von hohem Interesse. Zum anderen könnte die Entwicklung verwandter Stickstoffverbindungen mit modifizierter Struktur zu noch stabileren oder leistungsfähigeren Materialien führen. Außerdem eröffnet die effiziente Energiefreisetzung ohne umweltschädliche Abbauprodukte wie Kohlendioxid oder Stickoxide eine nachhaltige Alternative zu Kohlenwasserstoffen in Antriebs- oder Explosivstoffen. Zusammenfassend ist die erfolgreiche Synthese und Charakterisierung des neutralen Hexanitrogens C2h-N6 ein wissenschaftlicher Meilenstein, der neue Horizonte in der Chemie des Stickstoffs öffnet. Er zeigt eindrucksvoll, wie Kombination moderner experimenteller Techniken mit theoretischer Chemie dazu beitragen kann, bisher unerreichbare Moleküle zu erschließen.
Die daraus resultierenden Erkenntnisse können weitreichende Auswirkungen auf Energiespeicherung, Materialwissenschaft und Umweltverträglichkeit haben. Es bleibt spannend, inwieweit diese Entdeckung den Weg für praktische Anwendungen ebnen wird.






![Super Intelligence Speculation [video]](/images/F2DA8C40-9243-45A8-A826-F4540DD9CAD9)