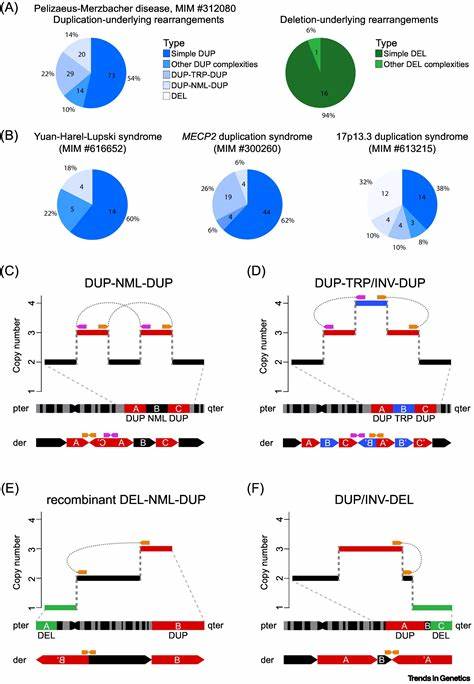
Die Forschung an neuen Stickstoffallotropen hat die wissenschaftliche Gemeinschaft lange Zeit fasziniert. Stickstoff, das mit einem Anteil von etwa 78 Prozent das Hauptbestandteil unserer Atmosphäre ist, hat in seiner üblichen molekularen Form N2 eine bemerkenswerte Stabilität und Inertheit. Doch die Suche nach höheren neutralen Stickstoffverbindungen, die mehr als zwei Atome enthalten, blieb eine Herausforderung, da diese aufgrund ihrer Instabilität oft nur von kurzer Dauer sind. Ein bedeutender Durchbruch in diesem Feld ist die erfolgreiche Synthese und Charakterisierung des neutralen Stickstoffallotrops Hexanitrogen mit der Symmetrie C2h-N6. Diese Entwicklung könnte die Türen zu neuen Energiekonzepten und innovativen Materialien aufstoßen.
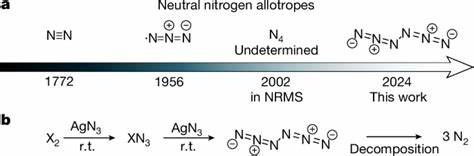
Hexanitrogen C2h-N6 ist ein Molekül, das ausschließlich aus Stickstoffatomen besteht und erstmals bei Raumtemperatur hergestellt werden konnte. Die Methode basiert auf der Reaktion von Silberazid (AgN3) mit halogenhaltigen Molekülen wie Chlor (Cl2) oder Brom (Br2). Diese Reaktion findet unter reduzierten Drücken statt, gefolgt von einer Abkühlung in Argon-Matrizen bei extrem niedrigen Temperaturen von 10 Kelvin. Dabei konnte N6 sowohl im Matrixisolationszustand als auch als reiner Film bei Flüssigstickstofftemperatur von 77 Kelvin stabil gehalten und analysiert werden.Die Herausforderungen bei der Herstellung neutraler Stickstoffallotrope liegen vor allem in ihrer energetischen Instabilität.
Die Bindungen in solchen Molekülen sind meist sehr schwach und brechen leicht auseinander, wobei die Typische Zerfallsroute in gewöhnliches molekulares Stickstoff (N2) mit hoher Exothermie verläuft. Bisher war es nur in wenigen Fällen möglich, koordiniert geladene Stickstoffpolymere oder flüchtige intermediäre Spezies wie das Azidradikal (•N3) oder N4 in der Gasphase nachzuweisen. Ein stabiles neutrales Molekül mit sechs Stickstoffatomen zu isolieren, wurde über Jahrzehnte als nahezu unmöglich angesehen.Das neu hergestellte N6 Molekül unterscheidet sich strukturell und elektronisch deutlich von bekannten Stickstoffverbindungen. Es weist eine C2h-Symmetrie auf und verfügt über eine acyclische Struktur, die zwei N3-Einheiten miteinander verknüpft.
Die Bindungslängen und die Analyse der Elektronendichte zeigen eine Mischung aus Doppel- und Einfachbindungen. Besonders auffällig ist, dass das zentrale N-N-Bindungspaar stabiler ist als erwartet, was die bemerkenswerte kinetische Stabilität guter Hunderte Millisekunden bei Raumtemperatur erklärt. Diese Stabilität wird durch eine energetische Barriere gegen den Zerfall in drei Moleküle N2 ermöglicht, die mit etwa 14,8 kcal/mol berechnet wurde.Die experimentelle Bestätigung erfolgte durch die Kombination fortschrittlicher Spektroskopieverfahren wie der Infrarotspektroskopie (IR) mit 15N-Isotopenmarkierung sowie UV-Vis-Spektroskopie. Diese Methoden lieferten klare Identifikationsmerkmale für das N6-Molekül und dessen Zerfallsmuster unter Lichteinwirkung.
Erfreulicherweise zeigte das Molekül auch unter den Bedingungen der Matrixisolierung sowie in reiner Filmform ohne Argon als Matrix geringe Zersetzung.Aus theoretischer Sicht wurde die Energielandschaft des Moleküls mit hochgenauen Quantenchemie-Methoden untersucht, darunter CCSD(T) Rechnungen mit großen Basissätzen. Dabei wurde bestätigt, dass nur die C2h-Form des Hexanitrogens ein stabiles Minimum auf der Potentialfläche darstellt, während andere Konfigurationen wie die C2v-Variante unbedeutend sind. Die elektronische Struktur wurde detailliert mittels Natural Bond Orbital-Analysen aufgeklärt, die Ladungsverteilungen und Bindungsordnungen abbilden. Diese Erkenntnisse unterstreichen das Potential von N6 als langlebiger, neutraler Stickstoffallotrop.
Die energetische Betrachtung des Zerfalls von N6 ist besonders vielversprechend: Die beim Zerfall freigesetzte Energie liegt weit über der von gängigen Treibstoffen und Explosivstoffen wie TNT oder HMX. Pro Gewichtsanteil setzt das Hexanitrogen fast das Doppelte an Energie frei. Auch in Bezug auf die Detonationsparameter übertrifft dieses Molekül klassische Energiematerialien wie RDX oder FOX-7 in bestimmten Aspekten. Diese Eigenschaften machen Hexanitrogen nicht nur in der fundamentalchemischen Forschung interessant, sondern eröffnen auch Perspektiven für Anwendungen in Hochenergiematerialien und sauberen Energiespeichern.Der Syntheseprozess basiert auf intelligent gesteuerten Gasphasenreaktionen und der gezielten Nutzung von Silberazid als Ausgangsstoff, der sich durch seine hohe Reaktivität gegenüber Halogen-Spezies als idealer Reaktionspartner erwiesen hat.
Die Reaktionen werden in Geräten wie Quarzrohren oder einfachen U-Fallen durchgeführt, unter präziser Kontrolle von Temperatur und Druck. Ein Schlüsselelement ist das sofortige Einfrieren der Reaktionsmischung in Matrixgasen bei ultrakalten Bedingungen, um das flüchtige N6 einzufangen und eine weitere Reaktion zu verhindern.Die Sicherheitsaspekte bei der Handhabung von Silberazid und Halogenaziden sind nicht zu unterschätzen. Aufgrund der hohen Explosivität dieser Verbindungen erfordert der Umgang sorgfältige Schutzmaßnahmen wie Blitzschutz, Sicherung gegen statische Entladung, und den Einsatz von Schutzkleidung. Ebenso sollten Experimente unter streng kontrollierten Bedingungen und in kleinen Mengen durchgeführt werden, um Risiken zu minimieren.
Ein weiterer bemerkenswerter Aspekt ist die Rolle von Quantenmechanischem Tunneln bei der Zersetzung des Moleküls. Während viele theoretisch vorhergesagte Stickstoff-Allotrope in kurzer Zeit zerfallen, zeigt das Hexanitrogen eine bemerkenswerte Resistenz gegenüber solchen Effekten, was seine potenzielle Stabilität in praktischen Anwendungen erhöht. Die theoretischen Halbwertszeiten betragen bei 77 K mehrere Jahre und selbst bei Raumtemperatur liegen sie im Bereich von Millisekunden, was ausreicht, um das Molekül im Labor zu untersuchen und zu verarbeiten.In der Zukunft könnten diese Erkenntnisse einen großen Einfluss auf die Entwicklung nachhaltiger Energiespeicher haben. Aufgrund der ausschließlich in der Molekülstruktur enthaltenen Stickstoffatome und der schadstofffreien Zersetzung in umweltfreundliches N2-Gas stellt Hexanitrogen eine ideale Grundlage für saubere Energiematerialien dar.
Die Herausforderungen liegen nun in der Skalierung der Synthese und in der Entwicklung praktischer Anwendungen, die von der hohen Energiedichte profitieren.Abschließend zeigt die erfolgreiche präparative Herstellung des neutralen Hexanitrogens C2h-N6, dass die langjährige Annahme von der Undurchführbarkeit neutraler höherer Stickstoffallotrope widerlegt ist. Mit moderner experimenteller Technik, unterstützt durch präzise theoretische Modelle, eröffnen sich neue Forschungsfelder im Bereich der chemischen Bindungen, der Energiematerialien und der Umweltverträglichkeit. Die Arbeit von Qian, Mardyukov und Schreiner ist ein Meilenstein, der die weitere Erforschung und Entwicklung hochenergetischer, aber dennoch stabiler Stickstoffverbindungen vorantreiben wird.





![Landing a Model Rocket [video]](/images/D194C2B9-6274-4785-88D0-5D268F0A3CB7)